Công nghiệp “Dược sinh học” và sinh phẩm
1. KHÁI NIỆM VÀ LỊCH SỬ PHÁT TRIỂN
1.1. Khái niệm
“Công nghiệp Dược Sinh học” (Biopharmaceutical industry) (bên cạnh công nghiệp Hóa Dược), là một nhánh của ngành Công nghiệp Dược Phẩm, chuyên sản xuất dược phẩm có nguồn gốc sinh học bằng công nghệ sinh học.
“Sinh phẩm” (Biopharmaceutical) là các dược phẩm có thành phần hoạt chất mang bản chất sinh học, được sản xuất bằng công nghệ sinh học.
- Theo Cơ quan Quản lý Thuốc và Thực phẩm Hoa Kỳ (US-FDA), “Sinh phẩm” (thuật ngữ là “Biologics”, “Biological product”) là nhóm chế phẩm đa dạng, thường là những đại phân tử, cấu trúc phức tạp. Những sản phẩm này được sản xuất bằng công nghệ sinh học từ nguồn sinh vật sống như vi sinh vật, tế bào thực vật/động vật và thường khó tiêu chuẩn hóa hơn so với các thuốc hóa dược (hoạt chất là các phân tử nhỏ)[1].
- Theo Cơ quan quản lý Thuốc của Châu Âu (EMA), “Sinh phẩm, Thuốc sinh học, Dược sinh học” (biological medicinal product) là các dược phẩm chứa hoạt chất được tạo ra hoặc dẫn xuất từ sinh vật sống[2].
- Theo Luật dược Việt nam 2016: “Sinh phẩm”(còn gọi là thuốc sinh học) là thuốc được sản xuất bằng công nghệ hoặc quá trình sinh học từ chất hoặc hỗn hợp các chất cao phân tử có nguồn gốc sinh học, bao gồm cả dẫn xuất của máu và huyết tương người. Sinh phẩm không bao gồm kháng sinh, chất có nguồn gốc sinh học có phân tử lượng thấp có thể phân lập thành những chất tinh khiết và sinh phẩm chẩn đoán in vitro[3].
1.2. Lịch sử phát triển
Công nghiệp “Dược Sinh học” bắt đầu được biết đến từ năm 1982, khi chế phẩm insulin (biệt dược Humulin) được sản xuất từ công nghệ tái tổ hợp ADN do Genentech/Eli Lilly nghiên cứu phát triển được cơ quan Quản lý Thuốc và Thực phẩm Hoa kỳ (US-FDA) phê duyệt và cấp phép làm thuốc điều trị đái tháo đường[4,5].
Kể từ đó đến nay, công nghiệp sản xuất “Sinh phẩm” đã có những bước phát triển vượt bậc để tạo ra nhiều sinh phẩm ứng dụng trong điều trị nhiều loại bệnh khác nhau và hầu như được ứng dụng trong mọi chuyên ngành (chẩn đoán, điều trị, dự phòng) của các lĩnh vực y tế (Y, Dược, Răng Hàm Mặt, Vệ Sinh Dịch Tễ, Y Tế Dự Phòng…).
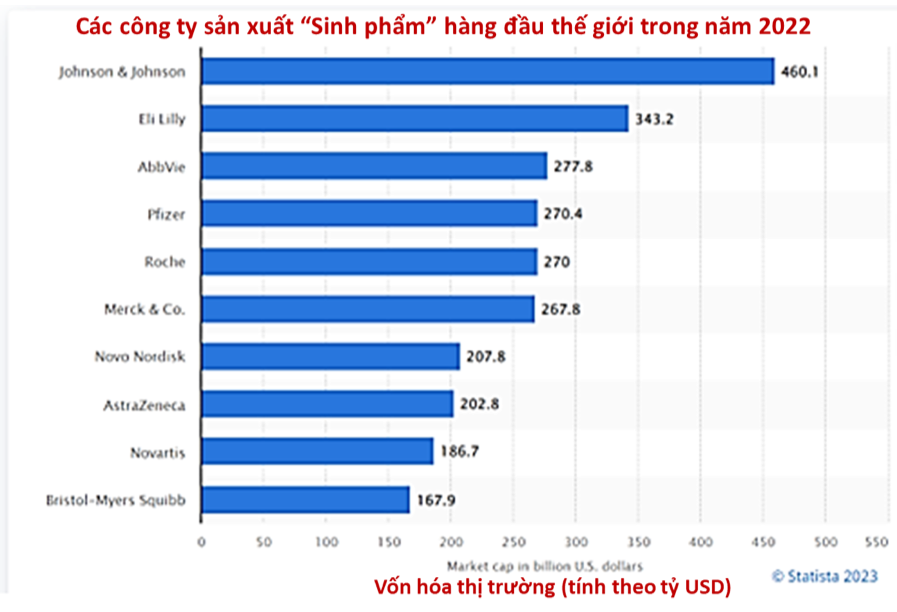
Trong những năm gần đây, thị trường “Dược Sinh học” gia tăng nhanh chóng, nhiều công ty dược phẩm lớn đã thành lập riêng nhánh “Dược Sinh học” và đầu tư vào nghiên cứu phát triển để tạo ra các sản phẩm mới. Theo trang thống kê Statista, những công ty có giá trị vốn hóa thị trường (Market Capitalization) cao nhất toàn cầu đầu tư cho lĩnh vực sản xuất “Sinh phẩm” trong năm 2022 bao gồm: Johnson & Johnson, Eli Lilly, AbbVie, Pfizer, Roche, Merck & Co., Novo Nordisk, AstraZeneca, Novartis, Bristol-Myers Squibb… (Biểu đồ 1), với tổng giá trị hơn 2.379 tỷ USD[6].
2. PHÂN LOẠI DƯỢC SINH HỌC/SINH PHẨM VÀ QUẢN LÝ CẤP PHÉP
2.1. Các nguồn nguyên liệu dùng để sản xuất “Dược Sinh học/Sinh phẩm”
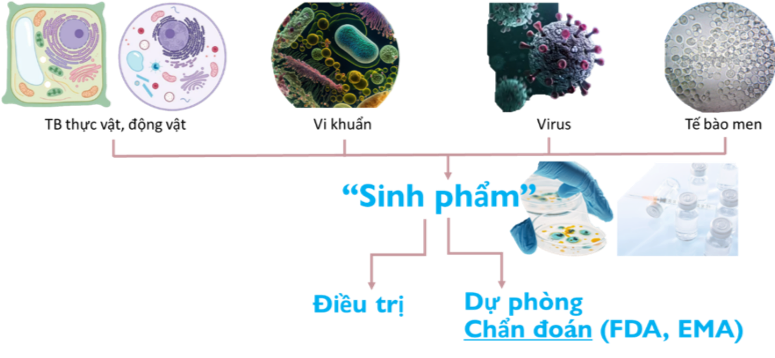
“Dược Sinh học/Sinh phẩm” có thể được sản xuất từ tế bào động vật, thực vật, vi khuẩn, virus hoặc tế bào men[1,2,4]. Phương pháp để bào chế có thể là phương pháp công nghệ sinh học cổ điển như nuôi cấy, chiết xuất, phân lập từ cơ thể sống của người, động vật, vi sinh vật hoặc ứng dụng các công nghệ sinh học tiên tiến như kỹ thuật tái tổ hợp ADN, kỹ thuật di truyền…[3]. Hiện nay, khi nói đến “Dược Sinh học/Sinh phẩm”, thường các công ty dược phẩm sẽ hướng đến các sản phẩm được sản xuất bằng công nghệ sinh học tiên tiến. Các “Dược Sinh học/Sinh phẩm” có thể được dùng cho mục đích điều trị bệnh, phòng bệnh và kể cả chẩn đoán (theo quy chế của US FDA và EMA)[1,2,4,5,7].
| Nguồn | Ví dụ | “Sinh phẩm” (công ty sản xuất), chỉ định |
| Tế bào thực vật | Tế bào cà-rốt
Hạt đậu (peanut) Arachis hypogaea L |
ELELYSOÒ – taliglucerase alfa (Protalix và Pfizer), điều trị bệnh Gaucher týp I
PALFORZIAÒ – bột đậu loại béo (Aimmune Therapeutics), điều trị dị ứng hạt đậu |
| Tế bào động vật | Tế bào biểu mô buồng trứng chuột
Tụy heo |
ACTIVASEÒ – alteplase (Genentech), làm tan cục máu đông trong đột quị não và nhồi máu cơ tim
Insulin (không còn sản xuất) |
| Vi khuẩn | E. coli
Bacillus clausii, … |
NEUPOGENÒ – filgrastim (Amgen), trị giảm bạch cầu do hóa trị, do thuốc
“PROBIOTICS” – chưa có chế phẩm nào được cấp phép ở dạng “Sinh phẩm” |
| Virus | Adenovirus
Rubella virus |
VAXZEVRIAÒ – (AstraZeneca), vaccine phòng covid-19
MERUVAXÒ – rubella virus sống (Merck Sharp & Dohme), vaccine phòng covid-19 |
| Tế bào nấm men | Saccharomyces cerevisiae | GARDASILÒ – kháng nguyên HPV (Merck), vaccine phòng ung thư do HPV |
2.2. Phân loại “Dược Sinh học/Sinh phẩm”
“Dược Sinh học/Sinh phẩm” có thể được phân loại theo quan điểm chung dựa trên nguồn nguyên liệu sản xuất và công nghệ sinh học áp dụng trong quá trình bào chế, sản xuất. Tuy nhiên, trên cơ sở quản lý, việc cấp phép một “Sinh phẩm” cần có những tiêu chuẩn rõ ràng và nghiêm ngặt vì thế không phải tất cả các chế phẩm nằm trong phân loại “Sinh phẩm” sẽ được cấp phép lưu hành nếu chưa thỏa mãn các yêu cầu của cơ quan quản lý.
2.2.1. Phân loại “Dược Sinh học/Sinh phẩm” theo quan điểm chung
Theo quan điểm chung, “Dược Sinh học/Sinh phẩm” là những sản phẩm chứa các hoạt chất là những phân tử lớn, cấu trúc phức tạp như các phân tử đường, protein, acid nucleic, tế bào sống, mô sống được đăng ký ở dạng thuốc và được sản xuất hoặc chiết xuất hoặc bán tổng hợp từ các nguồn sinh học (từ người, động vật và vi sinh vật) bằng các quy trình sinh học (kể cả chiết xuất) hoặc từ công nghệ tái tổ hợp ADN[5]. Như vậy theo định nghĩa này, “Dược Sinh học/Sinh phẩm” bao gồm những sản phẩm có nguồn gốc sinh học được bào chế theo các quy trình công nghệ cổ điển và các sản phẩm được bào chế theo công nghệ hiện đại, tân tiến nhất.
“Dược Sinh học/Sinh phẩm” cổ điển bao gồm các dạng được sản xuất tự nhiên hoặc không qua kỹ thuật tái tổ hợp hoặc là từ một nguồn sinh học (ví dụ các chế phẩm từ máu, các chiết xuất tự nhiên, các vaccin cổ điển và chế phẩm từ tế bào không qua xử lý công nghệ)[6].
Theo quan điểm định chuẩn của công nghệ sinh học và của các công ty “Dược Sinh học” hàng đầu trên thế giới, “Dược Sinh học/Sinh phẩm” hiện nay chủ yếu tập trung vào những sản phẩm được bào chế từ các quy trình công nghệ hiện đại như kỹ thuật tái tổ hợp và kỹ thuật gen[7].
Bảng 2. Phân loại “Dược Sinh học/Sinh phẩm” theo công nghệ bào chế[5]
| Chiết xuất từ hệ cơ thể sống | Từ kỹ thuật tái tổ hợp ADN |
| Chế phẩm từ máu người
– Máu toàn phần – Huyết tương tươi đông lạnh – Hồng cầu, … |
Kháng thể đơn dòng
– Trastuzumab (điều trị ung thư vú) – Rituximab (điều trị thấp khớp) |
| Chế phẩm từ mô người
– Gan, tim, thận: dùng trong ghép tạp |
Vaccine
– Covid-19 mRNA vaccin (Pfizer) |
| Chế phẩm từ tế bào gốc
– Tế bào gốc nước ối (tái tạo da, tim, thần kinh, …) – Tế bào gốc nhau thai (điều trị ung thư, thiếu máu) – Tế bào gốc tạo máu (điều trị ung thư máu, …) |
Các chất tương tự các protein, hormon, …, trong cơ thể
* Yếu tố đông máu – Thrombin (yếu tố 2) * Protein – Interferon, interleukin * Hormon – Insulin – Erythropoietin |
| Kháng thể chiết từ máu người
– Immunoglobulin IGIV (tăng cường miễn dịch) |
|
| Hệ vi sinh từ phân người
– Ghép phân (đưa hệ vi sinh ở phân người khỏe sang người bị bệnh đường tiêu hóa) |
|
| Tế bào sinh sản người
– Thụ tinh trong ống nghiệm |
Emzym trị liệu
– Collagenase – Alteplase |
| Chế phẩm từ động vật
– Insulin từ tụy heo (ngưng lưu hành) |
Bảng 3. Phân loại “Dược Sinh học/Sinh phẩm” theo bản chất và kỹ thuật sinh học sử dụng[7]
| “Dược Sinh học/Sinh phẩm” từ công nghệ tái tổ hợp, công nghệ chuyển gen |
| Yếu tố đông máu – tái tổ hợp ở tế bào
– Esperoct (VIII factor)/Novo Nordisk Yếu tố đông máu – ở động vật chuyển gen – Sevenfact (VIIa) – thỏ chuyển gen/Hema |
| Chống đông, chống huyết khối tái tổ hợp, chuyển gen
– TNKase (tenecteplase) tái tổ hợp /Roche-Genentech – Rocunest (C1 esterase inhibitor) ở thỏ chuyển gen/Pharming Americas |
| Hormon tái tổ hợp ở tế bào, men, vi khuẩn
– Rezvoglar (insulin glargine)/Eli Lilly – Sogroya (growth hormone)/Novo Nordisk – Rekovelle (FSH)/Ferring Pharmaceuticals – Sondelbay (parathyroid hormone)/Accord Healthcare |
| Interleukin, interferon, yếu tố hoại tử khối u tái tổ hợp ở vi khuẩn
– PEG-intron (interferon alpha)/Schering Plough – Extavia (interferon beta)/Novartis – Beromun (TNF alpha)/Belpharma |
| Vaccine tái tổ hợp, công nghệ gen
– PreHevbri (hetatitis B)/VBI vaccines – Comirnaty (covid-19)/Pfizer – Dengvaxia (Dengue)/Sanofi Pasteur |
| Kháng thể đơn dòng tái tổ hợp ở tế bào, vi khuẩn
– Alymsys (bevacizumab)/Amneal Pharmaceuticals – Vabysmo (faricimab)/Genentech – Tezspire (tezepelumab-ekko)/Amgen, AstraZeneca |
| Protein tái tổ hợp ở tế bào
– Infuse (bone morphogenetic protein)/Medtronic Sofamor Danek |
| Enzyme tái tổ hợp ở vi khuẩn, men, động vật chuyển gen
– Rylaze (asparaginase)/Jazz Pharmaceuticals – Nexviazyme (alpha-glucosidase)/Genzyme – Kanuma (sebelipase alpha)/Alexion |
| Protein dung hợp tái tổ hợp từ các gen khác nhau
– Nghenla (somatrogon)/Pfizer – Lumoxiti (moxetumomab, pasudotox)/AstraZeneca – Benepali (etanercept)/Samsung Bioepis |
| “Dược Sinh học/Sinh phẩm” từ gen, acid nucleic, SiRNA, antisense oligonucleotid |
| – Amvuttra (vutriSiRNA)/Alnylam
– Leqvio (casimersen)/Sarepta Therapeutics |
| “Dược Sinh học/Sinh phẩm” từ công nghệ tế bào |
| – Breyanzi (CD8, CD4, anti-CD19)/Bristol-Myers Squibb
– Carvykti (lympho T, anti-BCMA CAR)/Janssen Biotech |
2.2.2. Phân loại “Dược Sinh học/Sinh phẩm” theo quan điểm quản lý của FDA, EMA
Quản lý “Dược Sinh học/Sinh phẩm” theo cơ quan quản lý Thuốc và Thực phẩm Hoa Kỳ (FDA)
US FDA cấp phép “Dược Sinh học/Sinh phẩm” sau khi có đánh giá bởi Trung tâm Nghiên cứu và Đánh giá “Dược Sinh học/Sinh phẩm” (Center for Biologics Evaluation and Research – CBER) hoặc Trung tâm Nghiên cứu và Đánh giá Dược phẩm (Center for Drug Evaluation and Research – CDER) trực thuộc FDA. Tất cả hồ sơ liên quan đến đăng lý và xin cấp phép lưu hành sẽ thực hiện theo đúng hướng dẫn của CBER và CDER (mẫu đăng ký, hồ sơ kỹ thuật, …, có thể tải từ trang thông tin của CBER và CDER/FDA).[8]
US FDA phân loại và quản lý “Dược Sinh học/Sinh phẩm” theo các hạng mục sau:
“Dược Sinh học/Sinh phẩm” được cấp phép bởi CBER :
- Test dị ứng & Các sản phẩm điều trị dị ứng làm từ kháng nguyên (chó, mèo, côn trùng, đậu, phấn hoa, …
- Máu & Các sản phẩm từ máu
- Máu toàn phần
- Các phân đoạn từ huyết tương (albumin, các yếu tố đông máu, …)
- Thuốc thử xác định nhóm máu có bản chất là kháng thể
- Thuốc thử xét nghiệm virus truyền nhiễm qua máu (HIV, HBV, HCV, Cytomegalovirus, …)
- Thuốc thử xét nghiệm vi khuẩn truyền nhiễm qua máu (lậu, giang mai, …)
- Immunoglobulin
- Sản phẩm trị liệu từ Tế bào & Trị liệu gen
- Tế bào gốc
- Sản phẩm gen trị liệu ung thư
- Mô & sản phẩm từ Mô
- Xương, da, giác mạc, dây chằng, gân, van tim, …
- Tạng kèm mạch máu (tim, gan, thận, …) không do CBER quản lý và cấp phép
- Vaccine
- Hệ vi sinh từ phân người
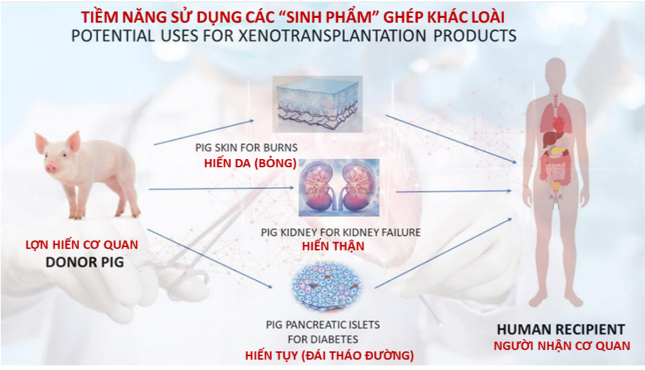
- Sản phẩm cấy ghép từ tế bào, mô, … ở loài khác sang người
- Da, tụy, …, từ heo ghép sang người
- Kháng thể đơn dòng
- Protein trị liệu (cytokine, enzymes, …)
- Thuốc điều hòa miễn dịch
- Hormon
Quản lý “Dược Sinh học/Sinh phẩm” theo Cơ quan Quản lý Thuốc Châu Âu (EMA)
Tương tự như US FDA, EMA cấp phép “Dược Sinh học/Sinh phẩm” sau khi có đánh giá bởi Ủy ban về Thuốc sử dụng cho người (Committee for medicinal products for human use – CHMP) và Ủy ban Thuốc Tân tiến (Committee for Advanced Therapies) trực thuộc EMA[9,10].
Các dạng chế phẩm được xếp vào “Dược Sinh học/Sinh phẩm” gồm:
- Máu, sản phẩm từ máu và Huyết tương
- Thuốc sản xuất từ công nghệ tái tổ hợp ADN
- Vaccine
- Thuốc điều trị tân tiến
- Trị liệu gen
- Trị liệu tế bào, mô
- Thuốc sản xuất từ công nghệ tế bào, mô
Quản lý và cấp phép “Sinh phẩm” ở Việt Nam
Ở Việt Nam, việc quản lý và cấp phép “Sinh phẩm” do Cục Quản Lý Dược, Bộ Y Tế chịu trách nhiệm. “Sinh phẩm” được đánh giá bởi các chuyên gia thẩm định và thông qua ý kiến tư vấn của Hội đồng Tư vấn cấp giấy đăng ký Vaccine và “Sinh phẩm” [11].
Các dạng chế phẩm được cấp phép trong kênh này bao gồm:
- Vaccine
- “Sinh phẩm” (bao gồm tất cả các chủng loại “Sinh phẩm” theo phân loại chung của FDA, EMA, NGOẠI TRỪ “Sinh phẩm” chẩn đoán
- Probiotics
3. “PROBIOTIC”
3.1. “Probiotic” là gì
Năm 2001, Tổ chức Y tế thế giới (WHO – World Health Organization) và Tổ chức Lương-Nông Liên hợp quốc (FAO – Food and Agriculture Orgarnization) đã thống nhất đưa ra định nghĩa cho “Probiotic”. Theo đó, “Probiotic” là những chế phẩm chứa các vi sinh vật sống khi sử dụng với lượng đủ sẽ mang lại lợi ích sức khỏe cho đối tượng sử dụng[12]. Cũng từ khi định nghĩa này ra đời, thuật ngữ “Probiotic” đã được sử dụng chưa thật sự chính xác, nếu không nói là đã lạm dụng quá mức. Đã có rất nhiều sản phẩm khai thác thuật ngữ “Probiotic” nhưng thật sự chất lượng của sản phẩm không đạt đúng yêu cầu của cơ quan quản lý. Chính vì thế các sản phẩm dạng “Probiotic” bắt đầu được các cơ quan quản lý chú ý hơn về việc cấp phép nhằm bảo vệ người tiêu dùng không bị dẫn dắt bởi các công bố vượt quá thực tế.
Tháng 10/2013 Hiệp hội Khoa học quốc tế về “Probiotic” và “Prebiotic” (The International Scientific Association for Probiotics and Prebiotics – ISAPP) bao gồm các chuyên gia về tiêu hóa, nhi, bác sĩ gia đình, vi sinh đường ruột, vi khuẩn tạo “probiotic”, vi sinh di truyền, miễn dịch và thực phẩm cùng với sự tham gia của các thành viên từ FAO/WHO đã tổ chức một hội nghị đồng thuận về phạm vi sử dụng thuật ngữ “Probiotic” và sử dụng hợp lý thuật ngữ này [13]. Hội nghị đã đưa ra những đồng thuận sau:
- Tiếp tục sử dụng định nghĩa của FAO/WHO về “Probiotic”.
- Phân biệt rõ hệ vi sinh hội sinh đường ruột với “Probiotic”: mặc dù hệ vi sinh hội sinh đường ruột là nguồn để tạo ra “Probiotic” nhưng nếu chưa xác định rõ chủng vi sinh để sản xuất ra “Probiotic” thì chưa được gọi hệ vi sinh này là “Probiotic”.
- Hệ vi sinh từ phân người vì thế không được xem là “Probiotic”.
- Một sản phẩm nếu công bố là một “Probiotic” thì cần phải xác định rõ chủng vi sinh đã được phân lập để sử dụng, các tiêu chuẩn đặc trưng và bằng chứng lâm sàng cho thấy mang lại lợi ích cho sức khỏe.
- Chứng minh được các tác động của “Probiotic”
3.2. Lợi ích của “Probiotic”
Dựa trên những kết quả thử nghiệm lâm sàng, các phân tích gộp và những bài tổng quan hệ thống về “Probiotic” hội nghị đồng thuận đã rút ra kết luận rằng “Probiotic” mang lại một số lợi ích nhất định cho sức khỏe. Dựa trên quy chế xét duyệt “Probiotic” của Cơ quan Y tế Canada (Health Canada)[14] và Ý, một số đồng thuận của hội nghị về chủng vi sinh sử dụng, liều lượng, …, áp dụng khi sử dụng “Probiotic” dưới dạng thực phẩm hoặc sản phẩm bổ sung chứ không phải ở dạng thuốc đã được thông qua[13]:
- Chủng vi khuẩn sử dụng: Bifidobacterium (adolescentis, animalis, bifidum, breve và longum) và Lactobacillus (acidophilus, casei, fermentum, gasseri, johnsonii, paracasei, plantarum, rhamnosus và salivarius)
- Liều: 1 x 109 CFU cho mỗi lần sử dụng
Bên cạnh các chủng trên, hiện nay một số chủng vi khuẩn và nấm men khác cũng được sử dụng làm “Probiotic”. Các chủng này bao gồm:
- Nấm men: Saccharomyces boulardii (chủng duy nhất được sử dụng làm “Probiotic”)[15]
- Vi khuẩn: Streptococcus thermophilus, Streptococcus salivarius, Enterococcus faecalis[16,17].
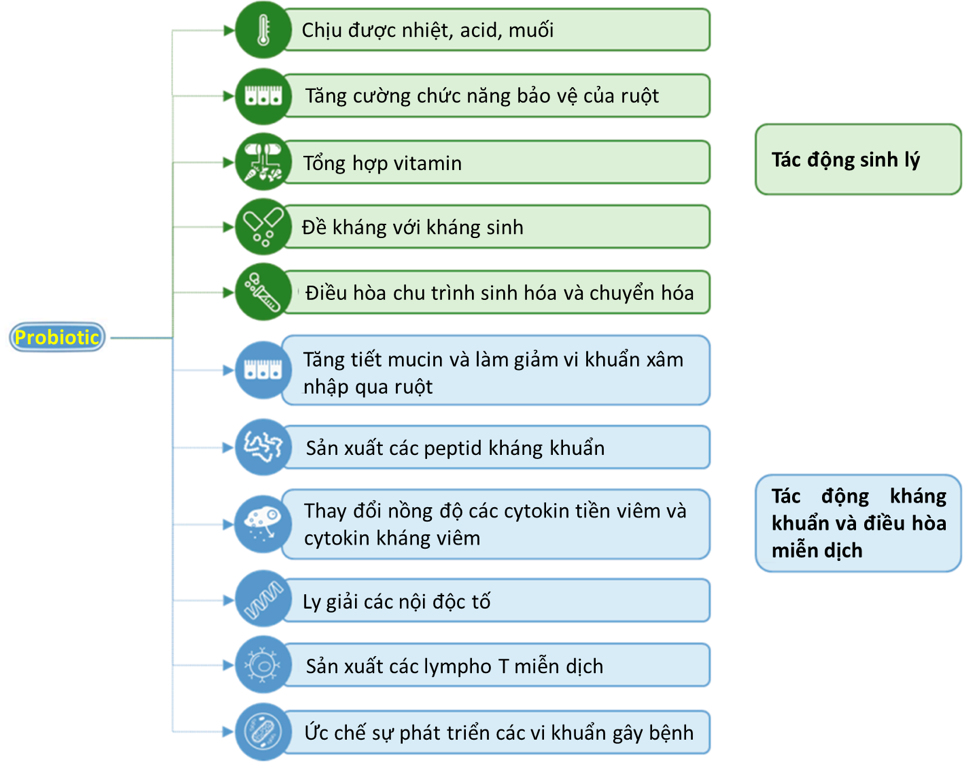
“Probiotic” đã được nghiên cứu trên nhiều tác động khác nhau và cho thấy lợi ích trên chức năng sinh lý và miễn dịch. Những lợi ích của “Probiotic” được minh họa trong hình 3.
3.3. Đánh giá tính an toàn của “Probiotic”
“Probiotic” là sản phẩm chứa vi sinh vật sống vì thế tính an toàn của “Probiotic” khi sử dụng làm sản phẩm bảo vệ sức khỏe cần được đánh giá chặt chẽ, xác định xem liệu sản phẩm có an toàn và có nguy cơ gây hại hay không. Tuy nhiên hiện nay, công tác đánh giá tính an toàn của “Probiotic” vẫn là một thách thức do thiếu bằng chứng về các đặc tính gây độc của các chủng sử dụng. Độc lực này có thể đặc hiệu theo từng chủng vi khuẩn vì thế càng khó khăn hơn.
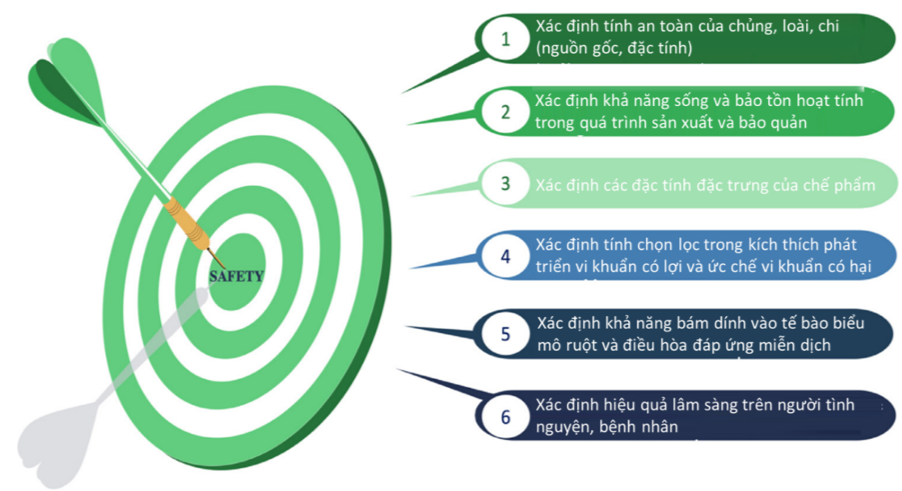
Để đảm bảo tính an toàn, các chủng vi sinh sử dụng trước hết phải không gây bệnh và không gây nguy cơ bất lợi nào cho đối tượng sử dụng. Hai chủng hiện được xem an toàn là Lactobacillus và Bifidobacteria. Ở Hoa Kỳ, Lactococcus lactis và Lactobacillus được xem là an toàn do sự hiện diện của chúng trong hệ vi sinh đường ruột[19]. Tuy nhiên, không phải tất các các loài trong cùng một chủng lại có đặc tính an toàn như nhau do chúng có thể tiết ra độc tố khác nhau, xâm nhập vào máu, lấy các đoạn gen gây bệnh trong môi trường ruột và chuyển sang bộ gen của các vi khuẩn gây bệnh, … Vì vậy, việc đánh giá tính an toàn của “Probiotic” cần được thực hiện dựa trên những tiêu chuẩn sau:
3.4. Các cách quản lý và cấp phép “Probiotic” ở một số nước trên thế giới
Với sự phát triển ngày càng đa dạng của các sản phẩm “Probiotic”, việc quản lý và cấp phép sản phẩm dạng này được nhiều cơ quan Y tế của nhiều nước quan tâm để tránh việc sử dụng sai và lạm dụng thuật ngữ “Probiotic” trên thị trường. Bên cạnh đó, việc bảo vệ người tiêu dùng tránh khỏi những công bố quá mức của các sản phẩm dạng “Probiotic” các cơ quan quản lý nhà nước đã thiết lập các kênh cấp phép cho “Probiotic” ở 3 dạng: thực phẩm chức năng, thuốc, “Dược Sinh học/Sinh phẩm”.
- Nếu một sản phẩm “Probiotic” công bố một tác dụng cụ thể dùng để phòng ngừa, điều trị một rối loạn/bệnh lý cụ thể thì hồ sơ sẽ được đánh giá và cấp phép ở dạng thuốc.
- Nếu một sản phẩm “Probiotic” không công bố một tác dụng cụ thể nào về mặt dược lý thì hồ sơ sẽ được đánh giá và cấp phép ở dạng thực phẩm bổ sung hoặc thực phẩm chức năng.
- Tương tự, một sản phẩm “Probiotic” không công bố bất kỳ tác dụng dược lý cụ thể nào và được tích hợp vào thức ăn (ví dụ phô-mai, sữa chua, …) hoặc thức uống (ví dụ sữa uống lên men Yakult, nước táo lên men, …) thì được xem là thực phẩm probiotic.
- Nếu một sản phẩm “Probiotic” đáp ứng các yêu cầu của một “Sinh phẩm” thì sẽ được cấp phép ở dạng “Dược Sinh học/Sinh phẩm”
Bảng 4. cung cấp thông tin cấp phép “Probiotic” ở một số nước trên thế giới.
Bảng 4. Quản lý “Probiotic” ở một số nước trên thế giới[19]
| TT | Quốc gia/ Khu vực | Phân loại Quản lý – Cấp phép | Cơ quan Quản lý và Cấp phép |
| 1 | Hoa Kỳ | – Thuốc
– Thực phẩm dinh dưỡng – “Dược Sinh học/Sinh phẩm” – Sản phẩm trị liệu chứa sinh vật sống – Thực phẩm y học |
US FDA
US FDA US FDA US FDA US FDA |
| 2 | Châu Âu | Thực phẩm chức năng | EFSA |
| 3 | Nhật Bản | – “Probiotic”
– Thực phẩm chức năng và bổ sung dinh dưỡng |
MHLW, FOSHU |
| 4 | Trung Quốc | – Thực phẩm chức năng | SFDA |
| 5 | Canada | – Sản phẩm sức khỏe thiên nhiên | FDA |
| 6 | Brazil | – Thực phẩm chức năng | ANVISA |
| 7 | Thái Lan | – Thực phẩm chức năng | FDA Thái Lan |
| 8 | Malaysia | – Thực phẩm chức năng | FSQD |
| 9 | Ấn độ | – Thực phẩm chức năng
– Thuốc |
FSSA
FDA |
| 10 | Việt Nam | – “Sinh phẩm”
– Thực phẩm bảo vệ sức khỏe/bổ sung dinh dưỡng |
DAV
VFA |
FDA (Food and Drug Administration): Cơ quan Quản lý Thuốc và Thực phẩm (của từng nước sở tại)
EFSA (European Food Safety Authority): Cơ quan Quản lý An toàn Thực phẩm Châu Âu
FAO/WHO=Food and Agricultural Organization/World Health Organization: Tổ chức Lương-Nông/Tổ chức Y tế thế giới
MHLW (Ministry of Health and Welfare): Bộ Y tế và Phúc lợi
FOSHU (Food for Specified Health Use): Thực phẩm sử dụng cho chức năng sức khỏe đặc thù
SFDA (State Food and Drug Administration): Cơ quan Quản lý Thuốc và Thực phẩm Quốc gia
ANVISA (National Health Surveillance Agency Brazil): Cơ quan Quản lý Y tế Brazil
FSQD (Food Safety and Quality Division): Cơ quan Kiểm soát Chất lượng và An toàn Thực Phẩm
FSSA (Family and Social Service Administration): Cơ quan Quản lý Dịch vụ Xã hội và Gia đình
VFA (Viet Nam Food Safety Authority): Cục An toàn Thực phẩm Việt Nam
DAV (Drug Administration of Viet Nam): Cục Quản lý Dược Việt Nam
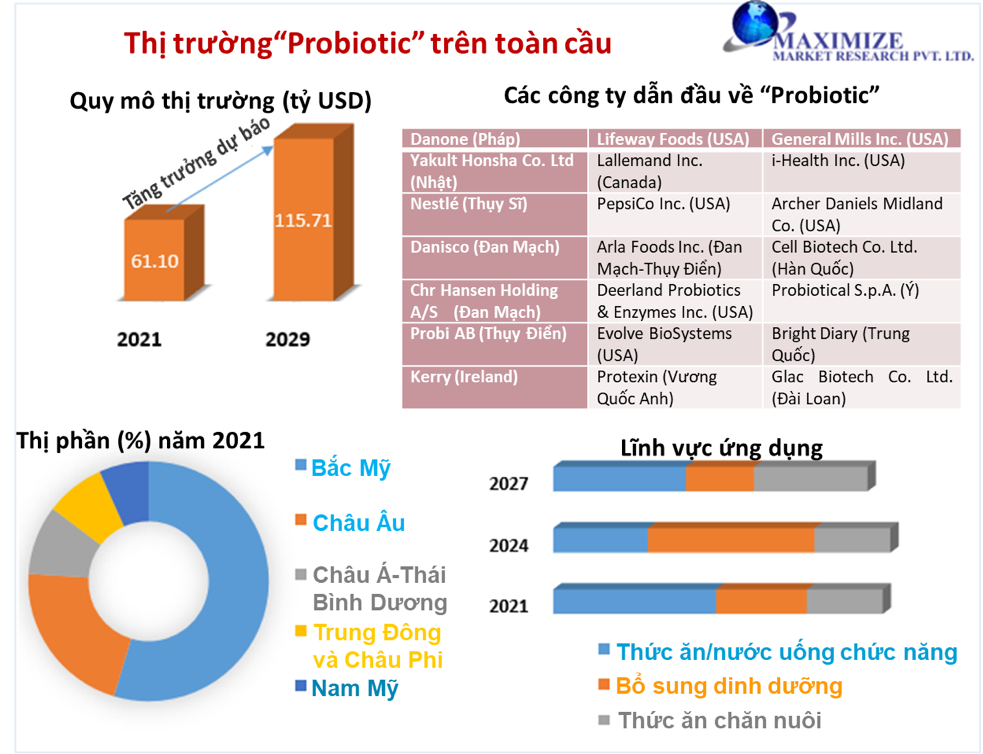
3.5. Tiềm năng của “Probiotic” trên thế giới
Nhật bản là quốc gia hàng đầu trên thị trường nghiên cứu, phát triển và tiêu thụ “Probiotic”. Đây là quốc gia đầu tiên áp dụng quy chế cấp phép các sản phẩm “Probiotic” ở 3 dạng: thực phẩm dinh dưỡng, thực phẩm chức năng và thực phẩm dùng cho chức năng sức khỏe đặc thù vào năm 1991.
Hoa kỳ cũng là một trong những quốc gia tạo thị trường mở cho “Probiotic” với các sản phẩm “Probiotic” sử dụng như một trị liệu thay thế (thuốc, “Sinh phẩm”) và cả dạng “Probiotic” thực phẩm.
Châu Âu bắt đầu áp dụng quy chế “Probiotic” thực phẩm chức năng trong năm 1995 và trở thành khu vực thứ 2 sau Nhật Bản phát triển thị trường “Probiotic” trong các loại sản phẩm từ sữa và nước uống.
Trung Quốc chỉ cấp phép “Probiotic” theo danh mục các chủng vi sinh vật riêng dưới dạng thực phẩm chức năng, tuy nhiên những yêu cầu về tính an toàn chưa được ban hành theo quy chế và chỉ cho phép công bố những tác dụng liên quan đến cải thiện chức năng về mặt sinh lý, chưa cho phép công bố những tác dụng mang tính dược lý.
Đối với các nước khối Đông Nam Á (ASEAN), thị trường “Probiotic” đang gia tăng về mặt nhu cầu nhập khẩu và sản xuất. Rất nhiều “Probiotic” dưới dạng thực phẩm dinh dưỡng, thực phẩm bảo vệ sức khỏe và thực phẩm chức năng được nhập khẩu vào khu vực này.
Trong năm 2021, thị trường “Probiotic” chiếm 61,1 tỷ USD và năm 2022 là 66,9 tỷ USD, dự báo sẽ đạt mức 73,14 tỷ USD trong năm 2023[20,21]. Với sự quan tâm của người tiêu dùng vào các loại thực phẩm tăng cường sức khỏe và các loại thực phẩm giàu dinh dưỡng, thị trường “Probiotic” sẽ tiếp tục được mở rộng. Khu vực Châu Á-Thái Bình Dương là thị trường “Probiotic” lớn nhất trong năm 2022, tiếp theo sau đó là khu vực Tây Âu, Bắc Mỹ [20,21].
- “Probiotic” dạng thức ăn và nước uống
- Các sản phẩm sữa
- Ngũ cốc
- Thực phẩm nướng (các loại bánh)
- Thịt lên men
- Thực phẩm khô
- “Probiotic” bổ sung dinh dưỡng
- Thức ăn bổ sung
- Dinh dưỡng bổ sung
- Bổ sung dinh dưỡng chuyên biệt
- Các công thức dinh dưỡng cho trẻ nhỏ
- “Probiotic” dùng trong chăn nuôi
3.6. Những ứng dụng trong sức khỏe hiện nay của “Probiotic”
3.6.1. Lợi ích của “Probiotics” trên sức khỏe tiêu hóa
Tiêu chảy do nhiễm khuẩn cấp ở trẻ em
Tiêu chảy cấp do nhiễm khuẩn ở trẻ em biểu hiện bởi tình trạng đi phân lỏng, đại tiện nhiều lần (ít nhất 3 lần/ngày) và có thể kèm theo sốt, nôn mữa. Tình trạng này có thể kéo dài đến 7 ngày. Bên cạnh các thuốc trị tiêu chảy được chỉ định cho trẻ em, “Probiotics” cũng được sử dụng khá phổ biến. Các bằng chứng từ hàng loạt nghiên cứu đã chứng minh được lợi ích của “Probiotics”.
Một phân tích tổng quan từ 63 thử nghiệm lâm sàng trên 8014 trẻ nhỏ và trẻ em cho thấy việc sử dụng “Probiotics” rút ngắn thời gian bị tiêu chảy do nhiễm khuẩn. Việc sử dụng sớm “Probiotics” làm giảm 59% nguy cơ tiêu chảy kéo dài hơn 4 ngày và giảm tần suất đại tiện xuống chỉ còn 1 lần/ngày vào ngày thứ 2 sau khi uống “Probiotics”[22].
Tiêu chảy do kháng sinh
Kháng sinh là một trong những nguyên nhân gây tiêu chảy cấp. Việc sử dụng kháng sinh làm rối loạn hệ vi sinh đường ruột, giảm tính đa dạng và làm giảm nhiều phản ứng chuyển hóa của hệ vi sinh đường ruột, vì thế thường dẫn đến tiêu chảy do thay đổi áp suất thẩm thấu ở ruột (gây quá dư thừa nước ở ruột). Bên cạnh đó, các vi khuẩn gây bệnh có cơ hội phát triển do không còn bị ức chế bởi hệ vi sinh đường ruột, nhu động ruột vì thế cũng tăng lên. Có khoảng 30% bệnh nhân sử dụng kháng sinh bị tiêu chảy. Trẻ em dưới 2 tuổi và người già trên 65 tuổi có nguy cơ tiêu chảy do kháng sinh cao hơn.
Các phân tích gộp và phân tích tổng quan từ 12 nghiên cứu lâm sàng với tổng số 1499 bệnh nhân từ trẻ em đến người lớn cho thấy “Probiotics” là giảm 51% nguy cơ bị tiêu chảy do kháng sinh. Tuy nhiên, việc dự phòng hoặc làm giảm tiêu chảy do kháng sinh lệ thuộc vào loại kháng sinh sử dụng và chủng vi sinh sử dụng trong “Probiotics”. Các chủng Lactobacillus và Saccharomyces có hiệu lực rõ rệt và trẻ em đáp ứng tốt hơn người lớn. Nếu “Probiotics” được sử dụng ngay trong vòng 2 ngày đầu sau khi sử dụng liều kháng sinh đầu tiên, hiệu quả dự phòng tiêu chảy do kháng sinh sẽ tốt hơn so với sử dụng “Probiotics” muộn[23].
Viêm ruột mạn tính
Viêm ruột mạn tính là tình trạng viêm kéo dài ở đại tràng (viêm đại tràng) và ruột non (bệnh Crohn). Có rất nhiều yếu tố liên quan đến viêm ruột mạn tính và một trong những yếu tố đó có thể là sự thay đổi hệ vi sinh đường ruột. Vì thế, bênh cạnh các thuốc kháng viêm steroid và nhiều thuốc khác, “Probiotics” cũng được nghiên cứu sử dụng.
Nhiều phân tích tổng quan và phân tích gộp đã phân tích các thử nghiệm lâm sàng và phần lớn đều đưa ra kết luận chung rằng: “Probiotics” mang lại lợi ích khi sử dụng cho bệnh nhân viêm đại tràng mạn tính nhưng ít hiệu quả trên bệnh Crohn.
Kết quả phân tích từ 17 thử nghiệm lâm sàng trên 1673 bệnh nhân trẻ em và người lớn bị viêm đại tràng cho thấy các “Probiotics” cải thiện triệu chứng ở bệnh nhân viêm đại tràng mức độ nhẹ-trung bình. “Probiotics” kết hợp với thuốc kháng viêm (5-ASA) có hiệu quả tốt hơn việc sử dụng thuốc kháng viêm 5-ASA một mình. Năm 2019, Hiệp hội Tiêu Hóa của Vương quốc Anh đã đưa “Probiotics” vào hướng dẫn điều trị viêm ruột mạn tính[24,25].
3.6.2. Lợi ích của “Probiotics” trên hệ miễn dịch
Đường tiêu hóa là một trong những hệ cơ quan trong đó sinh thái và hoạt động của hệ vi sinh đóng vai trò rất quan trọng lên hoạt động của hệ miễn dịch ở ruột. Trong hệ sinh thái này, việc sử dụng “Probiotics” sẽ kích thích hệ miễn dịch và tạo ra hệ thống truyền tin bởi các vi sinh đường ruột.
Trên tế bào biểu mô ruột
“Probiotic” tương tác với tế bào biểu mô ruột và do sự hiện diện ưu thế của chúng, các vi sinh trong “Probiotics” đóng vai trò như một cảm biến giúp ruột tương tác với môi trường. Các vi sinh trong “Probiotics” có thể đi vào tế bào ruột và hoạt hóa chuổi phản ứng của hệ miễn dịch (bao gồm các tế bào miễn dịch như đại thực bào, tế bào nhánh, tế bào lympho, …). “Probiotics” cũng đóng vai trò quan trọng trong việc kích hoạt và làm gia tăng số lượng tế bào tiết ở biểu mô ruột, dịch tiết này chứa nhiều peptid có tính kháng sinh và protein có tính miễn dịch giúp tăng cường hàng rào bảo vệ của ruột. Nhiều nghiên cứu cho rằng, “Probiotics” chỉ cần hiện diện trong khoảng 72 giờ là đủ để kích hoạt các tế bào tiết này và kích hoạt các đại thực bào, tế bào nhánh và các cytokine miễn dịch[26].
Ổn định cân bằng nội mô ruột
Một trong những đặc tính quan trọng của “Probiotic” là hoạt hóa hệ miễn dịch ruột nhưng không làm thay đổi cân bằng nội mô ruột. Điều này cho phép việc sử dụng “Probiotics” dài hạn mà không gây ra những tác động bất lợi và đảm bảo tính an toàn của “Probiotics”. Bên cạnh đó, các cytokine do các tế bào miễn dịch tiết ra dưới tác động của “Probiotics” sẽ làm tăng số lượng các tế bào sản xuất ra IgA. Các cytokine này cũng có thể kích hoạt các tế bào miễn dịch ở các cơ quan xa ruột như lách, màng bụng, niêm mạc hô hấp và cả tuyến sữa[26].
Cân bằng chức năng miễn dịch ngoài ruột
“Probiotic” có khả năng hồi phục cấu trúc giải phẩu tuyến ức và kích thích đáp ứng miễn dịch thích nghi trong quá trình suy dinh dưỡng. “Probiotics” cân bằng các loại lympho T giúp kiểm soát tiến trình dị ứng. Với tác động trên hệ miễn dịch ở ruột, các “Probiotics” có tác động điều hòa tính tự miễn ở ruột và toàn thân[26].
3.6.3. Lợi ích của “Probiotics” trên sức khỏe sinh sản
Trên sức khỏe sinh sản ở nam giới
Vai trò của hệ vi sinh trong tinh dịch: các nghiên cứu gần đây cho thấy tinh dịch chứa nhiều loại vi sinh khác nhau và có vai trò quan trọng trong duy trì chất lượng của tinh dịch. Các Lactobacillus trong tinh dịch giúp duy trì khả năng sống và di chuyển của tinh trùng. Hệ vi sinh ở tinh dịch có thể có nguồn gốc từ hệ vi sinh ở niệu đạo-sinh dục và cả từ hệ vi sinh ở ruột, miệng, máu hay cả ở âm đạo. Các vi sinh trong tinh dịch tương tác với tinh trùng trưởng thành và tác động đến chức năng của tinh trùng[27].
Hệ vi sinh trong truyến tiền liệt: tuyến tiền liệt là cơ quan hỗ trợ sinh sản quan trọng ở nam giới. Dịch tuyến tiền liệt không chỉ ảnh hưởng đến sự phóng tinh, hoạt hóa tinh trùng và giúp tinh trùng trưởng thành mà còn giúp tái tạo một số thành phần của đường sinh dục nữ và giúp chuẩn bị cho sự thụ tinh. Tuy nhiên, hệ vi sinh của tuyến tiền liệt vẫn chưa được nghiên cứu đầy đủ[28].
Lợi ích của “Probiotics” trên sức khỏe sinh sản nam giới: một số nghiên cứu tác động của “Probiotics” in vitro và in vivo cho thấy “Probiotics” làm tăng tính di động của tinh trùng cũng như nhiều thông số động học khác của tinh trùng. Chất lượng của tinh trùng và khả năng tạo tinh trùng tăng lên ở chuột thí nghiệm sau khi được cấy hệ vi sinh từ phân. Việc bổ sung “Probiotics” cũng giúp phục hồi lượng testosterone và khả năng sinh tinh ở chuột già. Một số nghiên cứu cho rằng, hệ vi sinh đường ruột làm tăng tính thấm qua hàng rào máu-tinh hoàn và giúp điều hòa chức năng của tinh hoàn. Do tác động có lợi của “Probiotics” trên tinh trùng, nhiều kết quả nghiên cứu trên động vật cho thấy “Probiotics” làm tăng số lượng con sinh ra, thể trọng khi sinh ra cũng cao hơn nhóm bình thường[29,30].
Trên sức khỏe sinh sản nữ giới
Vai trò của hệ vi sinh ở cơ quan sinh dục nữ: hệ vi sinh trong âm đạo nữ giới đóng vai tròng quan trọng trong ngăn chặn nhiễm trùng và điều hòa môi trường âm đạo. Bên cạnh âm đạo, gần đây, các nghiên cứu cho thấy có sự hiện diện của các vi sinh vật trong nang trứng, vòi trứng, tử cung và nhau thai.
Hệ vi sinh trong dịch nang trứng: hệ vi sinh này không khác biệt so với hệ vi sinh trong âm đạo, trong ruột và ở da. Sự hiện diện của hệ vi sinh trong dịch nang trứng có liên quan đến sự trưởng thành của phôi thai và chất lượng của phôi thai. Hệ vi sinh này cũng giúp bảo vệ trứng và giúp trứng trưởng thành nhờ tác động ngăn chặn sự phát triển của các vi sinh vật gây bệnh[31].
Hệ vi sinh trong tử cung và nhau thai: trước đây, tử cung và nhau thai được cho là môi trường không có sự hiện diện của vi sinh vật. Tuy nhiên những nghiên cứu gần đây cho thấy nhau thai chứa các vi sinh vật tương tự hệ vi sinh ở miệng và nội mạc tử cung. Ở trẻ sinh non, hệ vi sinh nhau thai có thành phần tương tự như ở âm đạo, cho thấy hệ vi sinh âm đạo có thể tác động đến chức năng nhau thai và ảnh hưởng đến kết quả sinh nở. Tương tự, tử cung cũng có hệ vi sinh riêng biệt và mang tính chuyển tiếp từ hệ vi sinh ở âm đạo (do cổ tử cung ngăn chặn sự xâm nhập của vi sinh vật từ âm đạo vào tử cung và một số vi sinh vật do tinh dịch mang vào). Hệ vi sinh trong tử cung có liên quan đến tình trạng hiếm muộn và xảy thai[32-35].
Hệ vi sinh trong âm đạo: là hệ vi sinh được xác định sớm nhất. Hệ vi sinh ở âm đạo chủ yếu là hội sinh trong đó chiếm ưu thế là Lactobacillus. Các chủng Lactobacillus tạo ra môi trường pH thích hợp để ngăn chặn sự phát triển của nấm và vi khuẩn, giúp cân bằng nội mô âm đạo. Sự thay đổi hệ vi sinh âm đạo có thể ảnh hưởng đến sự phát triển của bào thai và tình trạng mang thai[36-38].
Lợi ích của “Probiotics” trên sức khỏe sinh sản nữ giới: việc bổ sung “probiotics” có thể làm chậm sự ngưng hoạt động đột ngột của buồng trứng và giảm sản xuất estrogen ở phụ nữ mãn kinh vì thể, giảm các triệu chứng bốc hỏa, rối loạn lipid huyết và tăng cân. Việc sử dụng “Probiotics” cũng có thể làm tăng lượng FSH do đó kéo dài hoạt động của buồng trứng. Nhiều thí nghiệm trên động vật cho thấy “Probiotics” có tác động kích thích nang trứng phát triển và trưởng thành. Bên cạnh đó, việc sử dụng “Probiotics” làm tăng chức năng của nhau thai và các vi sinh trong “Probiotics” có thể đi vào trong nước ối của thai nhi. “Probiotics” cũng làm giảm nguy cơ tiền sản giật do làm giảm đáp ứng viêm ở nhau thai. Việc bổ sung “Probiotics” trong quá trình mang thai giúp điều hòa hệ vi sinh ở ruột và gây tác động có lợi cho sự phát triển của bào thai. Song song với các tác động có lợi trên sinh sản, “Probiotics” cũng giúp phòng ngừa một số bệnh lý ở hệ sinh sản như: giảm các triệu chứng của rối loạn chuyển hóa trong hội chứng buồng trứng đa nang, làm giảm nguy cơ viêm âm đạo, làm giảm nguy cơ viêm nội mạc tử cung[39-44].
3.6.4. Lợi ích của “Probiotics” trên sức khỏe răng miệng
Khoang miệng là hệ thống sinh thái năng động do dự thay đổi thường xuyên môi trường răng miệng và sự tương tác với nhiều yếu tố, trong đó có sự hiện diện của hệ vi sinh vật cộng sinh. Hệ vi sinh ở miệng không đồng nhất và đa dạng và sự mất cân bằng hệ này có thể gây nhiều bệnh răng miệng, điển hình như viêm nha chu hoặc “sâu rang”. “Probiotics” đối kháng và loại bỏ các mầm gây bệnh ở miệng, vì thế, có tác động dự phòng và điều trị một số bệnh ở miệng. Một phân tích gộp từ 361 nghiên cứu trên 5374 bệnh nhân có bệnh răng miệng cho thấy “Probiotics” ức chế các vi khuẩn gây bệnh. “Probiotics” cạnh tranh với vi khuẩn gây bệnh và làm tăng tỷ lệ các vi khuẩn có lợi trong miệng. Để có hiệu lực trên, “Probiotics” phải ở được trong khoang miệng, phải hỗ trợ hệ vi sinh ở khoang miệng và phải lưu trú được ở khoang miệng. Bên cạnh đó, “probiotics” phải không lên men đường làm thay đổi pH khoang miệng. “Probiotics” cũng phải có tác động làm giảm sản xuất các độc tố từ vi khuẩn, giảm sự tạo thành “biofilm”, ngăn chặn sự hình thành vôi răng qua tác động trên sự tiết nước bọt và tạo môi trường đệm trong khoang miệng.
Tác động của “Probiotics” trên hệ vi sinh ở miệng
Hệ vi sinh ở miệng giúp ngăn ngừa nhiều bệnh răng miệng. Vôi răng là mảng bám có thành phần là các tế bào vi khuẩn, các chất chuyển hóa, độc tố của vi khuẩn và các protein, polymer từ nước bọt và thức ăn tạo ra. Một số nghiên cứu cho thấy “Probiotics” ức chế sự tạo thành các mảng bám ở răng khi sử dụng “Probiotics” trong 2-3 tuần cho đến 3 tháng. Một số chủng vi sinh trong “Probiotics” vẫn còn tồn tại và kết dính trong khoang miệng cho đến 4 tháng sau khi ngưng uống, do đó, có thể cho tác dụng bảo vệ sâu răng kéo dài. Việc sử dụng “probitotics” cũng làm giảm các vi khuẩn gây bệnh răng miệng. Các nghiên cứu này cũng cho thấy rằng “Probiotics” không gây rối loạn hệ vi sinh ở miệng, một số có thể tồn tại kéo dài ở bề mặt răng và ngăn ngừa sâu răng[45-49].
Tác động của “Probiotics” trên nha chu
Viêm nha chu do các vi khuẩn gây bệnh hiện diện ở nha chu kết tập và tạo thành các “biofilm” ở nướu răng. Làm sạch vôi răng là biện pháp thông thường để loại bỏ các “biofilm” và kết hợp kháng sinh nếu có viêm. Các “Probiotics” có tác động ngăn chặn sự tái hình thành các “biofilm” do vi khuẩn tạo ra và làm thay đổi thành phần vi khuẩn gây bệnh trong “biofilm”, kể cả những “biofilm” hình thành cạnh các răng cấy ghép (implant). Tác động này là do hoạt tính ức chế phản ứng viêm, điều hòa miễn dịch và giảm hoạt tính các metalloproteinase[50-53].
Tác động của “Probiotics” trên nướu
Một phân tích gộp từ 14 thử nghiệm lâm sàng về việc sử dụng “Probiotics” trong điều trị viêm nướu răng và đánh giá sức khỏe nướu răng cho thấy sau 2-4 tuần sử dụng “Probiotics” tình trạng viêm nướu giảm, các chỉ số số viêm ở nướu và chỉ số vôi răng cũng giảm có ý nghĩa. Hiệu quả này tương tự như tác động của chlorhexidine. “Probiotics” cũng làm giảm số lượng vi khuẩn gây bệnh trong nước bọt. Hiện tượng chảy máu nướu răng giảm sau khoảng 4 ngày sử dụng. Các kết quả nghiên cứu này đưa ra kết luận: sử dụng “Probiotics” dài hạn có thể giúp cải thiện tình trạng vệ sinh răng miệng, tăng sức khỏe nướu răng và giảm viêm nướu[54-60].
Tác động của “Probiotics” trên viêm niêm mạc quanh vị trí cấy ghép
Viêm niêm mạc quanh vị trí cấy ghép là tình trạng viêm mô mềm quanh vị trí cấy ghép nhưng không đi kèm mất xương, chủ yếu do sự tạo “biofilm” của vi khuẩn gây bệnh. “Probiotics” có thể sử dụng để hỗ trợ điều trị do tác động ngăn chặn sự tạo thành biofilm. Các kết quả nghiên cứu lâm sàng chưa cho thấy hiệu quả đồng bộ của “Probiotics” trên viêm niêm mạc quanh vị trí cấy ghép do thiết kế nghiên cứu khác nhau. Vì vậy, cần có những kết quả nghiên cứu từ các thử nghiệm chặt chẽ và tiêu chuẩn để có thể rút ra kết luận về vai trò của “Probiotics” trong ngữ cảnh này[61-68].
Tác động của “Probiotics” trên “sâu răng”
“Sâu răng” là bệnh do nhiều yếu tố tạo ra và có liên quan đến độ pH trong khoang miệng do tác động của vi khuẩn hoặc thức ăn (thức ăn chứa đường). Do đặc tính kết dính vào khoang miệng và tồn tại kéo dài trong khoang miệng, ức chế vi khuẩn gây bệnh và ngăn chặn sự tạo “biofilm”, “Probiotics” đã được thử nghiệm trong điều trị hỗ trợ “sâu răng”. Các kết quả nghiên cứu cho thấy, ở trẻ em và trẻ nhỏ, “Probiotics” thể hiện tác động ngăn chặn “biofilm” ở giai đoạn sớm tốt hơn so với các “biofilm” đã hình thành quá lâu và giảm tỷ lệ “sâu răng”. Ở người lớn, “Probiotics” làm giảm số lượng vi khuẩn gây “sâu răng” và giúp các vi sinh trong “Probiotics” lưu trú trong hệ vi sinh miệng[69-78].
Tác động của “Probiotics” trên chứng hôi miệng
Hôi miệng là hiện tượng rất thường gặp ở trẻ em và cả người lớn. Hôi miệng có thể do ăn một số loại thức ăn, do vệ sinh răng miệng kém, viêm nha chu, nhiễm trùng hô hấp, hút thuốc lá, khô miệng hoặc do rối loạn hệ vi sinh ở miệng. Trong khoang miệng, sản phẩm chuyển hóa của các vi sinh vật ở dạng lưu huỳnh bay hơi sẽ gây hôi miệng. Một số yếu tố làm tăng sản phẩm chuyển hóa dạng này là vi khuẩn gram âm kỵ khí, pH nước bọt bị kiềm hóa, giảm thế oxy hóa-khử và sự hiện diện của các dẫn chất sulfuric như cysteine và methionine. Một số nghiên cứu cho thấy “Probiotics” làm giảm chứng hôi miệng sau khi điều trị trong vòng 4-12 tuần. Số lượng vi khuẩn sinh chất gây hôi giảm sau 4 tuần, tương tự nồng độ chất gây hôi cũng giảm tương ứng. Chỉ số cải thiện hôi miệng tăng sau 8 tuần. Ở các bệnh nhân bị hôi miệng do chỉnh hình răng, hiệu quả giảm hôi của “Probiotics” có thể đến muộn hơn (sau 1-3 tháng điều trị)[79-85].
4. KẾT LUẬN
Với công nghệ sản xuất hiện đại và định hướng đến các đích tác động cụ thể trong chẩn đoán, điều trị hoặc dự phòng một cách chọn lọc, “Dược Sinh học/Sinh phẩm” sẽ là thuốc của tương lai và là hướng phát triển chủ đạo của ngành công nghiệp dược phẩm.
Để phát triển công nghiệp “Dược Sinh học” cần đầu tư phát triển các kỹ thuật cao trong công nghệ sinh học như công nghệ di truyền, công nghệ tái tổ hợp… để có thể tạo ra các sản phẩm phát minh hoặc các “Sinh phẩm tương tự – Biosimilar” khi các sản phẩm gốc hết hạn bản quyền.
Trong các sản phẩm sản xuất từ nguồn sinh học, “Probiotic” cũng là một nhóm sản phẩm quan trọng. Với sự đa dạng về chủng loại và mức độ ứng dụng rộng rãi, “Probiotic” sẽ trở thành một định hướng chính trong công nghiệp dược phẩm, công nghiệp thực phẩm và chăn nuôi.
“Probiotic” là sản phẩm bảo vệ sức khỏe đầy tiềm năng cho hiện tại và tương lai. Việc sử dụng đúng “Probiotics” đem lại nhiều lợi ích trên sức khỏe tiêu hóa, sức khỏe sinh sản, sức khỏe răng miệng và tăng cường hệ miễn dịch của cơ thể.
Tuy nhiên, để có thể tạo ra những “Probiotic” được cả cơ quan quản lý và người tiêu dùng chấp nhận, các công bố về tác dụng sinh lý/tác dụng dược lý phải được chứng minh qua các thử nghiệm cần thiết. Bên cạnh đó, việc phát triển và áp dụng các phương pháp đánh giá chất lượng và tính an toàn của “Probiotic” cũng cần được thực hiện đầy đủ.
Biên soạn: PGS.TS. Trần Mạnh Hùng
Trưởng bộ môn Dược lý, Khoa Dược, ĐH Y Dược Tp. HCM
TÀI LIỆU THAM KHẢO
- US FDA – Biological product definition, fda.gov.
- EMA – Biological medicine, ema.europa.eu.
- Luật Dược Việt Nam – Luật số: 105/2016/QH13, https://luatvietnam.vn/y-te/luat-duoc-2016-104849-d1.html
- Kesik-Brodacka M. Progress in biopharmaceutical development. Biotechnol Appl Biochem. 2018 May;65(3):306-322. doi: 10.1002/bab.1617.
- Chen YC, Yeh MK. Introductory Chapter: Biopharmaceuticals. 2018 Sep 19. doi.org/10.5772/intechopen.79194.
- Mikulic M. Top biopharma companies worldwide by market cap Nov 2022. Statista 2023, https://www.statista.com/statistics/1258968/top-biopharmaceutical-companies-by-market-cap/#statisticContainer.
- Walsh G, Walsh E. Biopharmaceutical benchmarks 2022. Nat Biotechnol. 2022; 40(12):1722-1760. doi: 10.1038/s41587-022-01582-x.
- US FDA – Biologics regulated products, fda.gov.
- EMA – Committee for Advanced Therapies – CAT, ema.europa.eu.
- EMA – Committee for medicinal products for human use – CHMP, ema.europa.eu.
- Cục Quản Lý Dược, Bộ Y Tế, dad.gov.vn.
- Food and Agricultural Organization of the United Nations and World Health Organization. Health and nutritional properties of probiotics in food including powder milk with live lactic acid bacteria. World Health Organization, http://www.who.int/foodsafety/publications/ (2001).
- Hill C, Guarner F, Reid G, Gibson GR, Merenstein DJ, Pot B, Morelli L, Canani RB, Flint HJ, Salminen S, Calder PC, Sanders ME. Expert consensus document. The International Scientific Association for Probiotics and Prebiotics consensus statement on the scope and appropriate use of the term probiotic. Nat Rev Gastroenterol Hepatol. 2014; 11(8):506-14. doi: 10.1038/nrgastro.2014.66.
- Health Canada. Accepted Claims about the Nature of Probiotic Microorganisms in Food.
Health Canada, http://www.hc-sc.gc.ca/ (2009). - Kelesidis T, Pothoulakis C. Efficacy and safety of the probiotic Saccharomyces boulardii for the prevention and therapy of gastrointestinal disorders. Therap Adv Gastroenterol. 2012 Mar;5(2):111-25. doi: 10.1177/1756283X11428502.
- Poorni S, Srinivasan MR, Nivedhitha MS. Probiotic Streptococcusstrains in caries prevention: A systematic review. J Conserv Dent. 2019 Mar-Apr;22(2):123-128. doi: 10.4103/JCD.JCD_505_18.
- Krawczyk B, Wityk P, Gałęcka M, Michalik M. The Many Faces of Enterococcus-Commensal, Probiotic and Opportunistic Pathogen. Microorganisms. 2021 Sep 7;9(9):1900. doi: 10.3390/microorganisms9091900.
- Ghelardi E, Abreu Y Abreu AT, Marzet CB, Álvarez Calatayud G, Perez M 3rd, Moschione Castro AP. Current Progress and Future Perspectives on the Use of Bacillus clausii. Microorganisms. 2022 Jun 17;10(6):1246. doi: 10.3390/microorganisms10061246.
- Koirala S, Anal AK. Probiotics-based foods and beverages as future foods and their overall safety and regulatory claims. Future Foods 3. 2021; 100013.
- The Business Research Company – Probiotic global market report, https://www.thebusinessresearchcompany.com/report/probiotics-global-market-report.
- Maximize Market Research – Probiotics Market: Global Industry Analysis and Forecast (2022-2029), https://www.maximizemarketresearch.com/market-report/probiotics-market-size/542/
- Allen SJ, Martinez EG, Gregorio GV, Dans LF. Probiotics for treating acute
infectious diarrhoea. Cochrane Database Syst Rev 2010:CD003048. - Szajewska H, Kolodziej M. Systematic review with meta-analysis: Saccharomyces boulardii in the prevention of antibiotic-associated diarrhoea. Aliment Pharmacol Ther 2015;42:793-801.
- Su GL, Ko CW, Bercik P, Falck-Ytter Y, Sultan S, et al.. AGA clinical practice guidelines on the role of probiotics in the management of gastrointestinal disorders. Gastroenterology 2020; 159: 697-705.
- Derikx LA, Dieleman LA Hoentjen F. Probiotics and prebiotics in ulcerative colitis. Best Pract Res Clin Gastroenterol 2016; 30: 55-71.
- Maldonado Galdeano C, Cazorla SI, Lemme Dumit JM, Vélez E, Perdigón G. Beneficial Effects of Probiotic Consumption on the Immune System. Ann Nutr Metab. 2019;74(2):115-124.
- Altmäe S, Franasiak JM, Mändar R. The seminal microbiome in health and disease. Nat Rev Urol. 2019 Dec;16(12):703-721.
- Valcarce DG, Genovés S, Riesco MF, Martorell P, Herráez MP, Ramón D, Robles V. Probiotic administration improves sperm quality in asthenozoospermic human donors. Benef Microbes. 2017 Apr 26;8(2):193-206.
- Zhang P, Feng Y, Li L, Ge W, Yu S, Hao Y, Shen W, Han X, Ma D, Yin S, Tian Y, Min L, Sun Z, Sun Q, Zhang H, Zhao Y. Improvement in sperm quality and spermatogenesis following faecal microbiota transplantation from alginate oligosaccharide dosed mice. Gut. 2021 Jan;70(1):222-225.
- Poutahidis T, Springer A, Levkovich T, Qi P, Varian BJ, Lakritz JR, Ibrahim YM, Chatzigiagkos A, Alm EJ, Erdman SE. Probiotic microbes sustain youthful serum testosterone levels and testicular size in aging mice. PLoS One. 2014 Jan 2;9(1):e84877.
- Usman SF, Shuaibu IR, Durojaiye K, Medugu N, Iregbu KC. The presence of microorganisms in follicular fluid and its effect on the outcome of in vitro fertilization-embryo transfer (IVF-ET) treatment cycles. PLoS One. 2021 Feb 8;16(2):e0246644.
- Aagaard K, Ma J, Antony KM, Ganu R, Petrosino J, Versalovic J. The placenta harbors a unique microbiome. Sci Transl Med. 2014 May 21;6(237):237ra65.
- McElrath TF, Hecht JL, Dammann O, Boggess K, Onderdonk A, Markenson G, Harper M, Delpapa E, Allred EN, Leviton A; ELGAN Study Investigators. Pregnancy disorders that lead to delivery before the 28th week of gestation: an epidemiologic approach to classification. Am J Epidemiol. 2008 Nov 1;168(9):980-9.
- Moreno I, Garcia-Grau I, Perez-Villaroya D, Gonzalez-Monfort M, Bahçeci M, Barrionuevo MJ, Taguchi S, Puente E, Dimattina M, Lim MW, Meneghini G, Aubuchon M, Leondires M, Izquierdo A, Perez-Olgiati M, Chavez A, Seethram K, Bau D, Gomez C, Valbuena D, Vilella F, Simon C. Endometrial microbiota composition is associated with reproductive outcome in infertile patients. Microbiome. 2022 Jan 4;10(1):1.
- Moreno I, Codoñer FM, Vilella F, Valbuena D, Martinez-Blanch JF, Jimenez-Almazán J, Alonso R, Alamá P, Remohí J, Pellicer A, Ramon D, Simon C. Evidence that the endometrial microbiota has an effect on implantation success or failure. Am J Obstet Gynecol. 2016 Dec;215(6):684-703.
- Koedooder R, Mackens S, Budding A, Fares D, Blockeel C, Laven J, Schoenmakers S. Identification and evaluation of the microbiome in the female and male reproductive tracts. Hum Reprod Update. 2019 May 1;25(3):298-325.
- Wee BA, Thomas M, Sweeney EL, Frentiu FD, Samios M, Ravel J, Gajer P, Myers G, Timms P, Allan JA, Huston WM. A retrospective pilot study to determine whether the reproductive tract microbiota differs between women with a history of infertility and fertile women. Aust N Z J Obstet Gynaecol. 2018 Jun;58(3):341-348.
- Stout MJ, Zhou Y, Wylie KM, Tarr PI, Macones GA, Tuuli MG. Early pregnancy vaginal microbiome trends and preterm birth. Am J Obstet Gynecol. 2017 Sep;217(3):356.e1-356.e18.
- Brantsaeter AL, Myhre R, Haugen M, Myking S, Sengpiel V, Magnus P, Jacobsson B, Meltzer HM. Intake of probiotic food and risk of preeclampsia in primiparous women: the Norwegian Mother and Child Cohort Study. Am J Epidemiol. 2011 Oct 1;174(7):807-15.
- Rasool A, Alvarado-Flores F, O’Tierney-Ginn P. Placental Impact of Dietary Supplements: More Than Micronutrients. Clin Ther. 2021 Feb;43(2):226-245.
- Rasool A, Alvarado-Flores F, O’Tierney-Ginn P. Placental Impact of Dietary Supplements: More Than Micronutrients. Clin Ther. 2021 Feb;43(2):226-245.
- Li Y, Tan Y, Xia G, Shuai J. Effects of probiotics, prebiotics, and synbiotics on polycystic ovary syndrome: a systematic review and meta-analysis. Crit Rev Food Sci Nutr. 2023;63(4):522-538.
- Rostok M, Hütt P, Rööp T, Smidt I, Štšepetova J, Salumets A, Mändar R. Potential vaginal probiotics: safety, tolerability and preliminary effectiveness. Benef Microbes. 2019 Apr 19;10(4):385-393.
- Chenoll E, Moreno I, Sánchez M, Garcia-Grau I, Silva Á, González-Monfort M, Genovés S, Vilella F, Seco-Durban C, Simón C, Ramón D. Selection of New Probiotics for Endometrial Health. Front Cell Infect Microbiol. 2019 Apr 17;9:114.
- Thakkar PK, Imranulla M, Naveen Kumar PG, Prashant GM, Sakeenabi B, Sushanth VH. Effect of probiotic mouthrinse on dental plaque accumulation: A randomized controlled trial. Med Res. 2013, 1, 6.
- Burton, J.P.; Drummond, B.K.; Chilcott, C.N.; Tagg, J.R.; Thomson, W.M.; Hale, J.D.F.; Wescombe, P.A. Influence of the probiotic Streptococcus salivarius strain M18 on indices of dental health in children: A randomized double-blind, placebo-controlled trial. Med. Microbiol. 2013, 62, 875–884.
- Sarmento, E.G.; Cesar, D.E.; Martins, M.L.; de Oliveira Gois, E.G.; Furtado Martins, E.M.; da Rocha Campos, A.N.; Del’Duca, A.; de Oliveira Martins, A.D. Effect of probiotic bacteria in composition of children’s saliva. Food Res. Int. 2019, 116, 1282–1288.
- Rungsri, P.; Akkarachaneeyakorn, N.; Wongsuwanlert, M.; Piwat, S.; Nantarakchaikul, P.; Teanpaisan, R. Effect of fermented milk containing Lactobacillus rhamnosus SD11 on oral microbiota of healthy volunteers: A randomized clinical trial. Dairy Sci. 2017, 100, 7780–7787.
- Toiviainen, A.; Jalasvuori, H.; Lahti, E.; Gursoy, U.; Salminen, S.; Fontana, M.; Flannagan, S.; Eckert, G.; Kokaras, A.; Paster, B.; et al. Impact of orally administered lozenges with Lactobacillus rhamnosus GG and Bifidobacterium animalis subsp. lactis BB-12 on the number of salivary mutans streptococci, amount of plaque, gingival inflammation and the oral microbiome in healthy adults. Oral. Investig. 2015, 19, 77–83.
- Socransky, S.S.; Haffajee, A.D.; Teles, R.; Wennstrom, J.L.; Lindhe, J.; Bogren, A.; Hasturk, H.; van Dyke, T.; Wang, X.; Goodson, J.M. Effect of periodontal therapy on the subgingival microbiota over a 2-year monitoring period. I. Overall effect and kinetics of change. Clin. Periodontol. 2013, 40, 771–780.
- Hallstrom, H.; Lindgren, S.; Widen, C.; Renvert, S.; Twetman, S. Probiotic supplements and debridement of peri-implant mucositis: A randomized controlled trial. Acta Odontol. Scand. 2016, 74, 60–66.
- Hallstrom, H.; Lindgren, S.; Yucel-Lindberg, T.; Dahlen, G.; Renvert, S.; Twetman, S. Effect of probiotic lozenges on inflammatory reactions and oral biofilm during experimental gingivitis. Acta Odontol. Scand. 2013, 71, 828–833.
- Ince, G.; Gursoy, H.; Ipci, S.D.; Cakar, G.; Emekli-Alturfan, E.; Yilmaz, S. Clinical and Biochemical Evaluation of Lozenges Containing Lactobacillus reuteri as an Adjunct to Non-Surgical Periodontal Therapy in Chronic Periodontitis. Periodontol. 2015, 86, 746–754.
- Penala, S.; Kalakonda, B.; Pathakota, K.R.; Jayakumar, A.; Koppolu, P.; Lakshmi, B.V.; Pandey, R.; Mishra, A. Efficacy of local use of probiotics as an adjunct to scaling and root planing in chronic periodontitis and halitosis: A randomized controlled trial. Res. Pharm Pract 2016, 5, 86–93.
- Imran, F.; Das, S.; Padmanabhan, S.; Rao, R.; Suresh, A.; Bharath, D. Evaluation of the efficacy of a probiotic drink containing Lactobacillus casei on the levels of periodontopathic bacteria in periodontitis: A clinico-microbiologic study. Indian J. Dent. Res. 2015, 26, 462–468.
- Morales, A.; Gandolfo, A.; Bravo, J.; Carvajal, P.; Silva, N.; Godoy, C.; Garcia-Sesnich, J.; Hoare, A.; Diaz, P.; Gamonal, J. Microbiological and clinical effects of probiotics and antibiotics on nonsurgical treatment of chronic periodontitis: A randomized placebo- controlled trial with 9-month follow-up. Appl. Oral. Sci. 2018, 26, e20170075.
- Laleman, I.; Yilmaz, E.; Ozcelik, O.; Haytac, C.; Pauwels, M.; Herrero, E.R.; Slomka, V.; Quirynen, M.; Alkaya, B.; Teughels, W. The effect of a streptococci containing probiotic in periodontal therapy: A randomized controlled trial. Clin. Periodontol. 2015, 42, 1032–1041.
- Teughels, W.; Durukan, A.; Ozcelik, O.; Pauwels, M.; Quirynen, M.; Haytac, M.C. Clinical and microbiological effects of Lactobacillus reuteri probiotics in the treatment of chronic periodontitis: A randomized placebo-controlled study. Clin. Periodontol. 2013, 40, 1025–1035.
- Invernici, M.M.; Salvador, S.L.; Silva, P.H.F.; Soares, M.S.M.; Casarin, R.; Palioto, D.B.; Souza, S.L.S.; Taba, M., Jr.; Novaes, A.B., Jr.; Furlaneto, F.A.C.; et al. Effects of Bifidobacterium probiotic on the treatment of chronic periodontitis: A randomized clinical trial. Clin. Periodontol. 2018, 45, 1198–1210.
- Butera, A.; Gallo, S.; Maiorani, C.; Molino, D.; Chiesa, A.; Preda, C.; Esposito, F.; Scribante, A. Probiotic Alternative to
Chlorhexidine in Periodontal Therapy: Evaluation of Clinical and Microbiological Parameters. Microorganisms 2020, 9, 69. - Laleman, I.; Pauwels, M.; Quirynen, M.; Teughels, W. The usage of a lactobacilli probiotic in the non-surgical therapy of peri-implantitis: A randomized pilot study. Oral. Implants. Res. 2020, 31, 84–92.
- Lauritano, D.; Carinci, F.; Palmieri, A.; Cura, F.; Caruso, S.; Candotto, V. Reuterinos((R)) as adjuvant for peri-implant treatment: A pilot study. J. Immunopathol. Pharmacol. 2019, 33, 2058738419827745.
- Pena, M.; Barallat, L.; Vilarrasa, J.; Vicario, M.; Violant, D.; Nart, J. Evaluation of the effect of probiotics in the treatment of peri-implant mucositis: A triple-blind randomized clinical trial. Oral. Investig. 2019, 23, 1673–1683.
- Galofre, M.; Palao, D.; Vicario, M.; Nart, J.; Violant, D. Clinical and microbiological evaluation of the effect of Lactobacillus reuteri in the treatment of mucositis and peri-implantitis: A triple-blind randomized clinical trial. Periodontal. Res. 2018, 53, 378–390.
- Mongardini, C.; Pilloni, A.; Farina, R.; Di Tanna, G.; Zeza, B. Adjunctive efficacy of probiotics in the treatment of experimental peri-implant mucositis with mechanical and photodynamic therapy: A randomized, cross-over clinical trial. Clin. Periodontol. 2017, 44, 410–417.
- Flichy-Fernandez, A.J.; Ata-Ali, J.; Alegre-Domingo, T.; Candel-Marti, E.; Ata-Ali, F.; Palacio, J.R.; Penarrocha-Diago, M. The effect of orally administered probiotic Lactobacillus reuteri-containing tablets in peri-implant mucositis: A double-blind randomized controlled trial. Periodontal. Res. 2015, 50, 775–785.
- Ahmedbeyli, D.R.; Seyidbekov, O.S.; Dirikan, I.S.; Mamedov, F.Y.; Ahmedbeyli, R.M. Efficacy of probiotic application in the treatment and prevention of peri-implant mucositis. Stomatologiia 2019, 98, 20–24.
- Zhao, R.; Hu, H.; Wang, Y.; Lai, W.; Jian, F. Efficacy of Probiotics as Adjunctive Therapy to Nonsurgical Treatment of Peri-Implant Mucositis: A Systematic Review and Meta-Analysis. Pharmacol. 2020, 11, 541752.
- Hasslof, P.; West, C.E.; Videhult, F.K.; Brandelius, C.; Stecksen-Blicks, C. Early intervention with probiotic Lactobacillus paracasei F19 has no long-term effect on caries experience. Caries Res. 2013, 47, 559–565.
- Teanpaisan, R.; Piwat, S.; Tianviwat, S.; Sophatha, B.; Kampoo, T. Effect of Long-Term Consumption of Lactobacillus paracasei SD1 on Reducing Mutans streptococci and Caries Risk: A Randomized Placebo-Controlled Trial. J. 2015, 3, 43–54.
- Hedayati-Hajikand, T.; Lundberg, U.; Eldh, C.; Twetman, S. Effect of probiotic chewing tablets on early childhood caries–a randomized controlled trial. BMC Oral. Health 2015, 15, 112.
- Di Pierro, F.; Zanvit, A.; Nobili, P.; Risso, P.; Fornaini, C. Cariogram outcome after 90 days of oral treatment with Streptococcus salivarius M18 in children at high risk for dental caries: Results of a randomized, controlled study. Cosmet. Investig. Dent. 2015, 7, 107–113.
- Stensson, M.; Koch, G.; Coric, S.; Abrahamsson, T.R.; Jenmalm, M.C.; Birkhed, D.; Wendt, L.K. Oral administration of Lactobacillus reuteri during the first year of life reduces caries prevalence in the primary dentition at 9 years of age. Caries Res. 2014, 48, 111–117.
- Campus, G.; Cocco, F.; Carta, G.; Cagetti, M.G.; Simark-Mattson, C.; Strohmenger, L.; Lingstrom, P. Effect of a daily dose of Lactobacillus brevis CD2 lozenges in high caries risk schoolchildren. Oral. Investig. 2014, 18, 555–561.
- Sudhir, R.; Praveen, P.; Anantharaj, A.; Venkataraghavan, K. Assessment of the effect of probiotic curd consumption on salivary pH and streptococcus mutans counts. Med. J. 2012, 53, 135–139.
- Alamoudi, N.M.; Almabadi, E.S.; El Ashiry, E.A.; El Derwi, D.A. Effect of Probiotic Lactobacillus reuteri on Salivary Cariogenic Bacterial Counts among Groups of Preschool Children in Jeddah, Saudi Arabia: A Randomized Clinical Trial. Clin. Pediatr. Dent. 2018, 42, 331–338.
- Javid, A.Z.; Amerian, E.; Basir, L.; Ekrami, A.; Haghighi-zadeh, M.H. Effects of Short-term Consumption of Probiotic Yogurt on Streptococcus Mutans and lactobacilli Levels in 18-30 Years Old Students with Initial Stages of Dental Caries in Ahvaz City. Food Sci. Res. 2015, 2, 6.
- Mortazavi, S.; Akhlaghi, N. Salivary Streptococcus mutans and Lactobacilli levels following probiotic cheese consumption in adults: A double blind randomized clinical trial(*). Res. Med. Sci. 2012, 17, 57–66.
- Hampelska, K.; Jaworska, M.M.; Babalska, Z.L.; Karpinski, T.M. The Role of Oral Microbiota in Intra-Oral Halitosis. Clin. Med. 2020, 9, 2484.
- Ye, W.; Zhang, Y.; He, M.; Zhu, C.; Feng, X.P. Relationship of tongue coating microbiome on volatile sulfur compounds in healthy and halitosis adults. Breath Res. 2019, 14, 016005.
- Monedeiro, F.; Milanowski, M.; Ratiu, I.A.; Zmyslowski, H.; Ligor, T.; Buszewski, B. VOC Profiles of Saliva in Assessment of Halitosis and Submandibular Abscesses Using HS-SPME-GC/MS Technique. Molecules 2019, 24, 2977.
- Lee, D.S.; Lee, S.A.; Kim, M.; Nam, S.H.; Kang, M.S. Reduction of Halitosis by a Tablet Containing Weissella cibaria CMU: A Randomized, Double-Blind, Placebo-Controlled Study. Med. Food 2020, 23, 649–657.
- Benic, G.Z.; Farella, M.; Morgan, X.C.; Viswam, J.; Heng, N.C.; Cannon, R.D.; Mei, L. Oral probiotics reduce halitosis in patients wearing orthodontic braces: A randomized, triple-blind, placebo-controlled trial. Breath Res. 2019, 13, 036010.
- Suzuki, N.; Yoneda, M.; Tanabe, K.; Fujimoto, A.; Iha, K.; Seno, K.; Yamada, K.; Iwamoto, T.; Masuo, Y.; Hirofuji, T. Lactobacillus salivarius WB21–containing tablets for the treatment of oral malodor: A double-blind, randomized, placebo-controlled crossover trial. Surg. Oral. Med. Oral. Pathol. Oral. Radiol. 2014, 117, 462–470.
- Keller, M.K.; Bardow, A.; Jensdottir, T.; Lykkeaa, J.; Twetman, S. Effect of chewing gums containing the probiotic bacterium Lactobacillus reuteri on oral malodour. Acta Odontol. Scand. 2012, 70, 246–250.