I. Công nghệ BFS
1. BFS là gì?
- BFS (Blow-Fill-Seal) là công nghệ hiện đại nhất được ứng dụng trong sản xuất các sản phẩm vô trùng.
- BFS (Blow-Fill-Seal) là 1 qui trình khép kín, cho phép tạo bình chứa (bao bì ống), làm đầy (bơm hoạt chất) và hàn kín trong điều kiện vô trùng.
- Blow – Thổi: Một ống được đùn từ hạt nhựa nguyên chất. Một vật chứa được thổi thành hình bằng không khí vô trùng.
- Fill – Làm Đầy: Sau đó, vật chứa ngay lập tức được bơm đầy chất lỏng hoặc bán rắn với số lượng chính xác
- Seal – Hàn kín: Cuối cùng, thùng chứa được hàn kín, nắp được hình thành.
Toàn bộ quá trình B-F-S diễn ra trong khoảng 15s
Toàn bộ dây chuyền được tự động làm sạch, khử trùng và làm khô bằng không khí vô trùng
2. Ưu điểm nổi bật của công nghệ BFS?
- BFS làm giảm tối đa sự can thiệp của con người trong quá trình sản xuất, giúp giảm nguy cơ nhiễm vi sinh vật và các vi tạp lạ
- BFS thích hợp để sử dụng các chế phẩm đòi hỏi vô trùng nghiêm ngặt như thuốc tiêm, thuốc nhỏ mắt, các sản phẩm sinh học, vắc xin…
- BFS đáp ứng tiêu chuẩn sản xuất thuân thủ GMP
- BFS được công nhận bởi cục quản lý dược của tất cả các nước tiên tiến nhất thế giới.
3. Xu hướng sản xuất sản phẩm bằng công nghệ BFS
- BFS được cấp bằng sáng chế năm 1963 và chiếc máy BFS đầu tiên ra đời năm 1964.
- Ngay từ ban đầu, công nghệ này đã chủ yếu phục vụ mục tiêu sản xuất các thuốc vô trùng.
- Ngày nay, BFS cho thấy, công nghệ này rất thích hợp và tạo ra sự tối ưu khi sản xuất các sản phẩm thuốc tiêm truyền, thuốc nhỏ mắt… đặc biệt là các sản phẩm sinh học.
- Công nghệ ưu việt và tiên tiến, tuy nhiên cần mức chi phí đầu tư cao, vậy nên BFS vẫn xuất hiện khiêm tốn tại Việt Nam.
Meracine là số rất ít những công ty dược phẩm đầu tư cho dây chuyền công nghệ này.
4. Công nghệ BFS và ứng dụng sản xuất men vi sinh dạng ống
- Đảm bảo vô trùng
- Không chất bảo quản
- Tiện dụng
II. Đánh giá chủng vi sinh probiotic (đặc chủng)
1. Định nghĩa/Quy định chung
Probiotic là những vi sinh vật sống, khi được cung cấp với số lượng đầy đủ sẽ mang lại lợi ích sức khỏe cho vật chủ.
- Quy định của FDA:
- Các quy định hiện hành của Hoa Kỳ phụ thuộc phần lớn vào mục đích sử dụng của sản phẩm. Probiotics thường nằm trong thành phần thực phẩm và thực phẩm bổ sung. Tuy nhiên, probiotic cũng có thể được sử dụng như dược phẩm.
- Quy định về Probiotics trong thực phẩm bổ sung
- Ban hành danh sách các chủng được sử dụng theo DSHEA (1998)
- Các chủng mới được phân lập gần đây có thể không được quy định theo DSHEA và có thể được coi là Thành phần mới trong bổ sung chế độ ăn uống (New Dietary Ingredient).
- Vào năm 2016, FDA đã chỉ định Enterococcus faecium, Enterococcus faecalis và Escherichia coli là vi khuẩn cần tránh trong TPCN. Tuy nhiên, bất chấp hướng dẫn của FDA, các chất bổ sung chế độ ăn uống có chứa Enterococcus faecium và/hoặc Enterococcus faecalis vẫn được bán trên thị trường dưới dạng ‘men vi sinh’ ở Hoa Kỳ.
- Quy định về probiotic trong thuốc
- Cần tiến hành các thử nghiệm lâm sàng để chứng minh cả tính an toàn và hiệu quả trước khi đưa ra thị trường.
- Quy định tại châu Âu:
- Việc sử dụng bất kỳ sinh vật nào trong danh sách làm nguyên liệu thực phẩm ở Liên minh Châu Âu không yêu cầu sự chấp thuận trước khi đưa ra thị trường của EFSA miễn là các chủng mới đáp ứng tiêu chí QPS (Qualified Presumption of Safety) (QPS là một hệ thống đánh giá chung được EFSA sử dụng để đánh giá an toàn trước khi đưa ra thị trường đối với các nhóm vi sinh vật được chọn sử dụng trong sản xuất thực phẩm và thực phẩm chức năng (EFSA, 2007); đánh giá bao gồm các mối lo ngại về an toàn cho con người, động vật và môi trường. Trong quá trình này, các chuyên gia đánh giá danh tính phân loại của vi sinh vật, khối lượng kiến thức/tài liệu liên quan và các mối lo ngại tiềm ẩn về an toàn. )
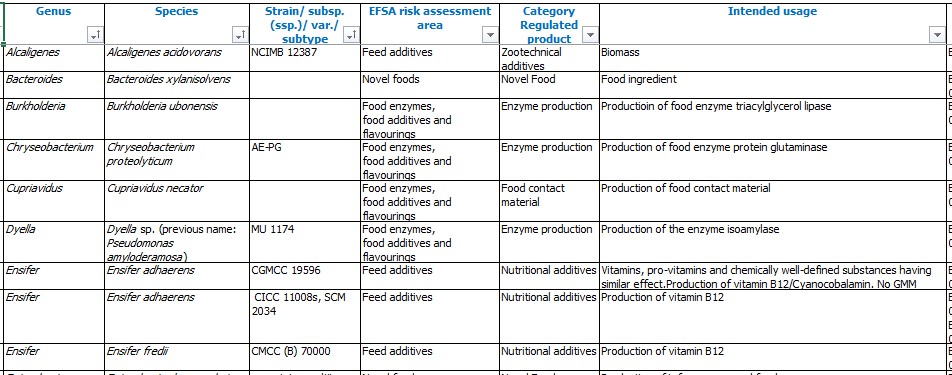
- Đưa ra danh sách các vi sinh vật có trạng thái QPS
2. Tiêu chí đánh giá chủng vi sinh (đặc chủng)
-
- Theo quy tắc nghiên cứu và định danh các vi sinh vật, các vi sinh vật được phân nhóm từ lớn đến nhỏ (Chi – Loài – Chủng). Theo khuyến cáo WHO, các lợi khuẩn bổ sung cần xác định chính xác và phân lập tới chủng. Ví dụ:
Việc phân loại tới chủng lợi khuẩn (định danh ở cấp độ chính xác nhất) liên quan trực tiếp đến lợi ích sức khỏe cũng như độ an toàn mà probitic mang lại.
- Cơ sở để Phân loại chủng:
- Đơn vị phân loại cơ bản ở vi khuẩn là loài (species). Các vi khuẩn trong cùng loài có cùng nguồn gốc, genotype, các tính chất sinh học và di truyền. Các loài rất gần nhau được xếp thành chi (genus), nhiều chi gần nhau hợp thành một họ (family), các họ gần nhau thành một bộ (order). Dưới loài là chủng (strain), chủng là tập hợp các tế bào con cháu của một khuẩn lạc đơn độc từ một quần thể thuần khiết. Các chủng thường được phân loại dưới mức loài bằng cách định kiểu huyết thanh, định kiểu enzyme, xác định độc tố hoặc các yếu tố độc lực khác hoặc đặc điểm của plasmid, kiểu protein hoặc acid nucleic.
- Gọi tên một vi khuẩn xác định gồm tên chi và tên loài. Mã quốc tế về danh pháp của vi khuẩn đã được quy định bởi ủy ban Quốc tế về Phân loại Vi khuẩn (International Committee on Systematic Bacteriology: ICSB). Tên chủng đặt theo tên tác giả tìm ra hoặc theo địa danh hoặc theo số hiệu kiểm tra. Tên chủng viết hoa.
- Ví dụ: Bộ: Spirochaetales Họ: Spirochaetaceae Chi: Treponema Loài: T. pallidum Chủng: Nicohn
- Danh sách QPS được ban hành bởi EFSA đưa ra các danh sách cụ thể đến chủng và lợi ích sức khỏe của chúng
- Nhận dạng/định danh chủng probiotic (đặc chủng)
- Các loài vi sinh vật sử dụng làm chế phẩm sinh học cho người (probiotic): hầu hết các chủng vi khuẩn sinh lactic (LAB) và bifidobacteria được sử dụng.
- Nhận dạng chủng vi sinh vật (đặc chủng): cần kết hợp kiểm tra kiểu hình và kiểu gen. Thông tin ẩn trong bộ gen của một chủng vi khuẩn là cơ sở để mô tả đầy đủ đặc điểm của chủng và để khám phá kỹ lưỡng các cơ chế và tiềm năng của nó.
- Kiểm tra kiểu hình: dựa vào đặc điểm nuôi cấy, một số tính chất chuyển hóa, các đặc điểm về hình thái
– Đặc điểm hình thái: tế bào, khuẩn lạc, quả thể, hình thức hoặc cơ quan sinh sản…
– Đặc điểm sinh lý, sinh hóa: khả năng sinh trưởng ở các điều kiện nuôi cấy khác nhau (pH, nhiệt độ), khả năng sử dụng các nguồn đường và sinh các enzyme bằng kit sinh hóa API 20NE, 20E, 50CH…
=> Phương pháp này có hạn chế do biến đổi kiểu hình đã được quan sát thấy ở nhiều loài vi khuẩn.
-
- Phương pháp phân tử để định danh vi khuẩn (kiểm tra kiểu gen): giải trình tự đoạn ITS, trình tự gen 16S rRNA, 18S rRNA, 26S rRNA hoặc các gen chức năng khác; phân tích trình tự hệ genome (whole genome sequencing).
=> Được coi là tiêu chuẩn vàng để phân định và mô tả các loài vi khuẩn mới, nhưng không thực tế (khó mở rộng và áp dụng) đối với xác định nuôi cấy các vi khuẩn thông thường
– Phân tích trình tự của gen 16S ribosome RNA (rRNA) là phân tích phổ biến được coi như là công cụ đầu tiên để định danh vi khuẩn: Tiến hành giải trình tự gen 16S rRNA so sánh ngân hàng cơ sở dữ liệu nhưu Phòng thí nghiệm sinh học phân tử châu Âu (http://www.ebi.ac.uk/embl/) hay Ngân hàng gen (http://www.ncbi.nlm.nih.gov/genbank/). Trình tự bộ gen hoàn chỉnh của hàng ngàn chủng vi khuẩn cho phép nhận dạng vi khuẩn mang tính chính xác và tin cậy cao
-
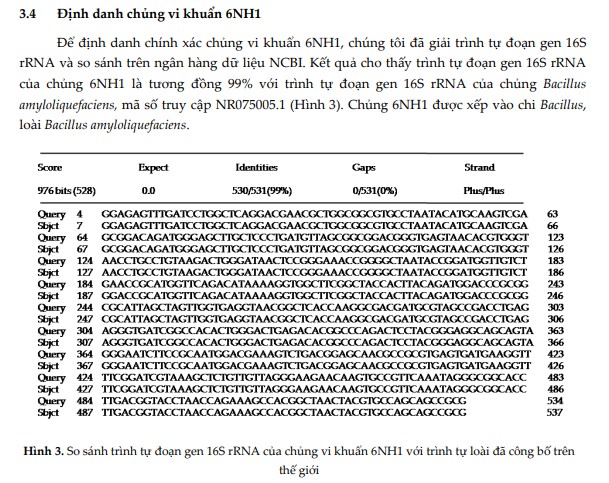
- Ví dụ: Trong nghiên cứu “Phân lập, tuyển chọn và định danh vi khuẩn có khả năng phân giải cellulose để sản xuất phân hữu cơ vi sinh”, Tạp chí Khoa học Đại học Huế:Nông nghiệp và Phát triển nông thôn; ISSN 2588–1191, Tập 127, Số 3A, 2018, Tr. 117–127
Tiến hành định danh bằng cách giải mã trình tự gen 16S rRNA, sau đó so sánh trên cơ sở dữ liệu gen. à Định danh chủng (Hình ảnh)
3. Đánh giá Probiotics trong thực phẩm
Tài liệu tham khảo
- [1] Hướng dẫn đánh giá Probiotics trong thực phẩm (2002) của tổ chức FAO/WHO
- [2] Huys G (2013), Microbial characterization of probiotics–advisory report of the Working Group “8651 Probiotics” of the Belgian Superior Health Council (SHC), Mol Nutr Food Res, 57(8):1479-504.
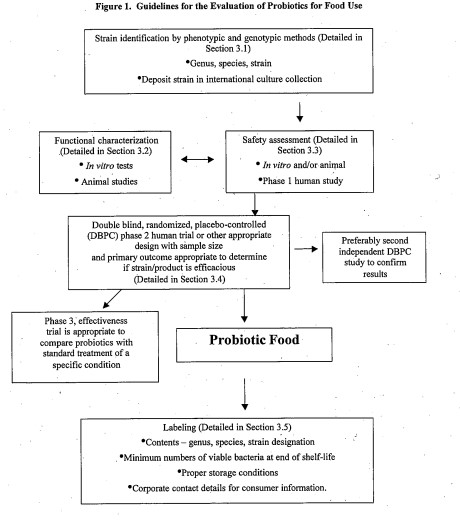
3.1. Sơ đồ chung
Gồm các bước:
- Xác định chính xác loài và phân loại chủng vi khuẩn và nấm men
- Các thử nghiệm trong ống nghiệm để sàng lọc các chủng lợi khuẩn tiềm năng: ví dụ như khả năng chống lại acid dạ dày, acid mật và các enzym tiêu hóa, hoạt tính kháng khuẩn chống lại vi khuẩn có khả năng gây bệnh, v.v…;
- Đánh giá độ an toàn: các yêu cầu để chứng minh rằng một chủng lợi khuẩn là an toàn
- Nghiên cứu in vivo để chứng minh các ảnh hưởng sức khỏe ở vật chủ mục tiêu
- Ghi nhãn
3.2. Các bước cụ thể
3.2.1. Xác định Chi/Loài/Chủng
- Chi/loài/chủng của probitic liên quan trực tiếp đến lợi ích sức khỏe cụ thể mà probitic mang lại. Ví dụ: S.themophilus, L.delbrueckii ssp.bulgaricus giúp tăng tiêu hóa lactose trên đối tượng không dung nạp lactose
- Xác định chi/loài/chủng của probiotic là rất cần thiết.
Danh mục các vi sinh vật có thể tham khảo tại:
– Apprpved Lists of Bacterial Names (In.J. Syst. Bacteriol, 1980, 30-225-420) also available in http://www.bacterio.cict.fr/
– Validation Lists, published in the International Journal of Systematic and Evolutionary Microbiology (or International Journal of Systermatic Bacteriology, prior to 2000)
- Phương pháp xác định: kết hợp kiểm tra kiểu hình và kiểu gen
3.2.2. Thử nghiệm sàng lọc chủng lợi khuẩn tiềm năng
Bao gồm các thử nghiệm in vitro sau: Tính kháng acid dạ dày; Tính kháng dịch mật; Tính bám dính vào dịch nhầy/biểu mô tế bào; Tính kháng khuẩn chống lại các vi khuẩn có khả năng gây bệnh; Khả năng giảm sự bám dính bề mặt của mầm bệnh; Hoạt tính thủy phân muối mật; Kháng chất diệt tinh trùng (ứng dụng cho âm đạo)
3.2.3. Đánh giá độ an toàn
- Tổng quan chung
- Các vi sinh vật được sử dụng trong quá trình sản xuất lên men thực phẩm có lịch sử sử dụng an toàn lâu dài và thường được gọi là vi sinh vật “cấp thực phẩm” hoặc GRAS (Được công nhận chung là an toàn). Do đó, hầu hết các chủng vi khuẩn sinh lactic (LAB) và bifidobacteria được sử dụng.
- Ở châu Âu, các chủng cần đáp ứng QPS (giả định đủ điều kiện về an toàn) (Danh mục các vi sinh vật có trạng thái QPS).
- Tuy nhiên ngay cả khi với các chủng LAB (thường được coi là có hồ sơ an toàn rất tốt) vẫn có thể tồn tại các nguy cơ: nhiễm trùng toàn thân, các hoạt động trao đổi chất có hại, kích thích miễn dịch quá mức trên đối tượng nhạy cảm và chuyển vị gen. (ví dụ: quan sát thấy viêm nội tậm mạc hay nhiễm trùng cơ hội ở những người bị suy giảm miễn dịch khi sử dụng Lactobacillus)
- Cách đánh giá: Cần thực hiện tối thiểu các test sau:
- Tính kháng kháng sinh: thực hiện thông qua thử nghiệm tính nhạy cảm với kháng sinh (phương pháp: khuếch tán đĩa thạch (lớp phủ), pha loãng canh thang và pha loãng thạch,…
- Các hoạt động trao đổi chất liên quan sản xuất các chất độc hại (ví dụ: liên hợp acid mật của vật chủ tạo ra acid mật thứ cấp – chúng có thể biểu hiện khả năng gây ung thư bằng cách tác động lên các tế bào tiết chất nhầy và thúc đẩy sự tăng sinh của chúng, hoặc chúng có thể đóng vai trò là chất thúc đẩy quá trình sinh ung thư…)
- Độc lực và đặc tính gây bệnh: sàng lọc trong ống nghiệm về sự tương tác của vi sinh vật với các dòng tế bào để điều tra các tác động gây độc tế bào hoặc bệnh lý tế bào có thể xảy ra sau khi phát triển trong các môi trường khác nhau, để biết sự hiện diện của các gen độc lực đã biết (ví dụ: hoạt động lecithinase, gen độc tố) và sự hiện diện của yếu tố di truyền di động.
- Hoạt tính kết tập tiểu cầu và hoạt tính phân hủy chất nhầy: Hoạt động tổng hợp tiểu cầu đã được coi là một thử nghiệm bắt buộc trong việc đánh giá mức độ an toàn của chế phẩm sinh học. Sự kết tập tiểu cầu bởi vi khuẩn được cho là góp phần vào sự tiến triển của viêm nội tâm mạc nhiễm trùng.
- Đánh giá các tác dụng không mong muốn thông qua các thử nghiệm trên người
- Giám sát dịch tễ học các phản ứng bất lợi ở người tiêu dùng (hậu mãi)
- Khác:
- Các thông số an toàn “đang được tranh luận”: sự hình thành, bám dính và chuyển vị (liên quan đến quá trình lây nhiễm và xâm lấn: sự tiếp xúc hoặc bám dính đầu tiên giữa các chủng vi khuẩn và tế bào biểu mô, sự di chuyển xa hơn của chủng vào hoặc xuyên qua biểu mô ruột và sự tăng sinh ở vị trí vô trùng của cơ thể, hoặc tại mức độ của lớp đệm, các hạch bạch huyết mạc treo, hoặc toàn thân dẫn đến nhiễm trùng huyết, viêm nội tâm mạc và nhiễm khuẩn huyết)
- Vi sinh vật biến đổi gen: rủi ro kháng kháng sinh, tích lũy môi trường, biến đổi gen của chúng sang sinh vật khác, đòi hỏi các biện pháp và giám sát cụ thể để đảm bảo an toàn.
3.2.4. Nghiên cứu in vivo để chứng minh các ảnh hưởng sức khỏe ở vật chủ mục tiêu
- Thử nghiệm chứng minh lâm sàng bao gồm đầy đủ các phae: Phase 1 (xác định liều an toàn), Phase 2 (hiệu quả), Phase 3 (so sánh hiệu quả và độ an toàn của phương pháp điều trị mới với phương pháp điều trị hiện có); Phase 4 (tiến hành sau khi thuốc đã được lưu hành)
- Probiotic sử dụng trong thực phẩm không cần thực hiện Phase 3 vì không có liệu pháp chuẩn để so sánh.
3.2.5. Ghi nhãn
- Lợi ích sức khỏe dựa trên các bằng chứng khoa học cụ thể cho phép việc ghi nhãn. Ví dụ: “Giảm tiêu chảy ở trẻ sơ sinh do rota virus”; “Tăng cường sức khỏe đường ruột”.
- Khuyến nghị ghi nhãn:
- Chi, loài và ký hiệu chủng.
- Số lượng khả thi tối thiểu của mỗi chủng lợi khuẩn khi hết thời hạn sử dụng;
- Khẩu phần được đề xuất phải cung cấp liều lượng men vi sinh hiệu quả liên quan đến yêu cầu về sức khỏe)
- Lợi ích sức khỏe (công dụng)
- Điều kiện bảo quản thích hợp
- Chi tiết liên lạc của công ty cho thông tin người tiêu dùng.
III. Sản phẩm men vi sinh
- Dạng bào chế phù hợp
- Chủng vi sinh chuyên biệt đảm bảo tác dụng
- Kiểm soát chất lượng sản phẩm cuối cùng (end-product)
- Tính xác thực của chủng và tính ổn định di truyền của chủng vi sinh
- Thành phần vi sinh vật: Thành phẩm thường chứa 107 – 109 CFU/ml (hoặc g)
- Độ ổn định của vi sinh vật:
– Điều kiện sản xuất phù hợp từng chủng vi sinh
– Điều kiện bảo quản: tuân thủ
- Sự nhiễm vi sinh vật (nhiễm vi sinh): không nhiễm vi sinh vật ngoại lai
- Dán nhãn và công bố